Qual a ação da substância do Soliqua?
Resultados de Eficácia
Resumo dos Estudos Clínicos
A segurança e eficácia de Lixisenatida + Insulina Glargina no controle da glicemia foram avaliadas em dois estudos clínicos randomizados em pacientes com diabetes mellitus tipo 2, em combinação a antidiabéticos orais (virgens de insulina) e substituição à insulina basal.
Em cada um dos estudos controlados com ativos, o tratamento com Lixisenatida + Insulina Glargina proporcionou melhora clínicas e estatística significativas na hemoglobina A1c (HbA1c).
Alcançar níveis mais baixos de HbA1c e alcançar uma maior redução de HbA1c não aumentou as taxas de hipoglicemia com o tratamento combinado versus a insulina glargina isolada
No estudo clínico de combinação com a metformina, a dose inicial foi de 10 unidades. No estudo clínico de substituição à insulina basal, a dose inicial foi de 20 ou 30 unidades, dependendo da dose anterior de insulina. Em ambos estudos, a dose foi titulada uma vez por semana, com base na média dos valores automonitorizados da glicemia de jejum a partir dos últimos 3 dias, de acordo com a Tabela 1 a seguir.
Tabela 1 – Algoritmo de titulação da dose de Lixisenatida + Insulina Glargina:
Glicemia de jejum automonitorizada (mg/dL) [mol/L] | Alteração da dose (unidades/dia) |
> 140 [> 7,77] | + 4 |
> 100 e ≤ 140 [> 5,55 e ≤ 7,77] | + 2 |
< 80 a 100 [4,44 a 5,55] | Sem alteração |
< 80 [< 4,44] | - 2 |
Estudo clínico em pacientes com diabetes tipo 2 não controlada com tratamento antidiabético oral
Em combinação com antidiabéticos orais (virgens de insulina)
Um total de 1.170 pacientes com diabetes tipo 2 foram randomizados em um estudo aberto, de 30 semanas, controlado com ativo, para avaliar a eficácia e segurança de Lixisenatida + Insulina Glargina em comparação aos componentes individuais, insulina glargina (100 unidades/mL) e lixisenatida.
Os pacientes com diabetes tipo 2, tratados com metformina isoladamente ou metformina e um segundo tratamento com antidiabético oral que poderia ser uma sulfonilureia ou uma glinida ou um inibidor de cotransportador-2 sódio glicose (SGLT-2) ou um inibidor de dipeptidil-peptidase-4 (DPP-4), e que não foram adequadamente controlados com este tratamento (variação de HbA1c de 7,5% a 10% para pacientes previamente tratados com metformina isoladamente e 7,0% a 9% para pacientes previamente tratados com metformina e um segundo tratamento antidiabético oral) entraram em tratamento (run-in) por um período de 4 semanas.
Durante esta fase (run-in), o tratamento com metformina foi otimizado e quaisquer outros antidiabéticos orais foram descontinuados. No final deste período (run-in), os pacientes que permaneceram inadequadamente controlados (HbA1c entre 7% e 10%) foram randomizados para Lixisenatida + Insulina Glargina, insulina glargina ou lixisenatida. No total, 58% dos pacientes na triagem receberam um segundo antidiabético oral.
A população com diabetes tipo 2 apresentava as seguintes características:
- A idade média era de 58,4 anos;
- 50,6% era do sexo masculino;
- 90,1% era caucasiano;
- 6,7% era negro ou afro-americano;
- 19,1% era hispânico.
A média do IMC no início do estudo foi de 31,7 kg/m2. A duração média do diabetes era de aproximadamente 9 anos.
Na Semana 30, Lixisenatida + Insulina Glargina proporcionou uma melhora estatisticamente significativa na HbA1c (valor de p < 0,0001) em comparação aos componentes individuais. Em uma análise pré-especifica de desfecho primário, as diferenças observadas foram consistentes em relação à HbA1c na linha basal (< 8% ou ≥ 8%) ou a utilização de antidiabéticos orais no início do tratamento (metformina isolada ou metformina mais um segundo antidiabético oral).
Tabela 2 – Resultados em 30 semanas – Estudo clínico de combinação com a metformina (população mITT (intenção de tratamento)):
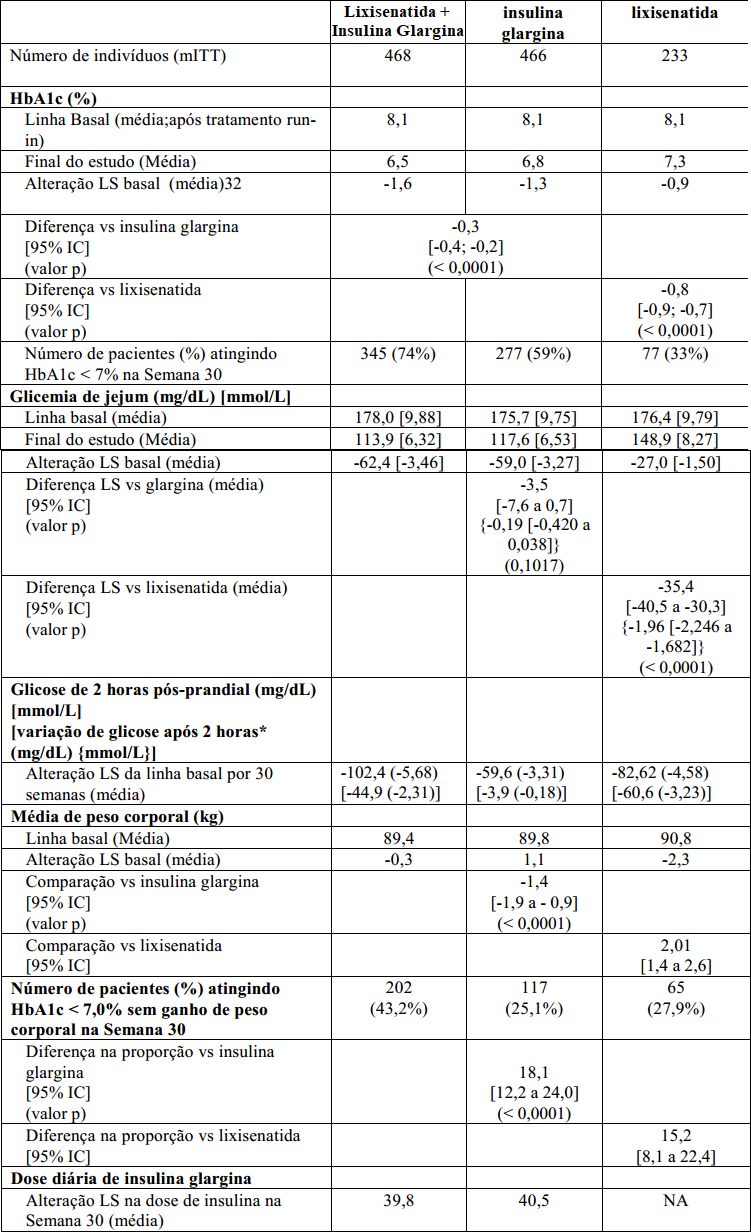
* Glicose de 2 horas pós-prandial menos o valor da glicose pré-refeição.
Figura 1 – HbA1c média (%) no início da triagem, ponto de randomização e em cada ponto de tempo (concluído) e na Semana 30 (LOCF*) - população mITT:
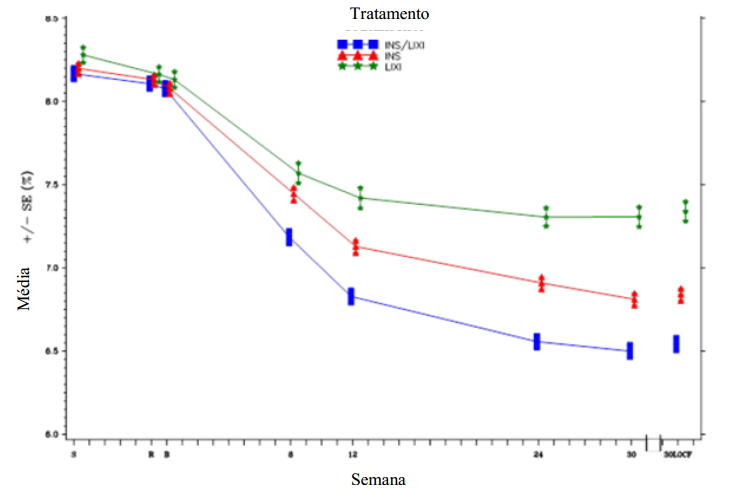
*LOCF = última observação realizada.
Os pacientes do grupo o qual fez uso de Lixisenatida + Insulina Glargina relataram diminuição estatisticamente significativa maior no perfil médio de 7 pontos SMPG a partir do início do tratamento até a Semana 30 (-60,36 mg/dL [-3,35 mmol/L]) em comparação aos pacientes do grupo que fez uso de insulina glargina (-47,87 mg/dL [-2,66 mmol/L]); diferença de 12,49 mg/dL [-0,69 mmol/L]) e ao grupo de pacientes que fez uso de lixisenatida (-35,11 mg/dL; diferença de 25,24 mg/dL) [(-1,95 mmol/L; diferença -1,40 mmol/L)] (p < 0,0001 para ambas comparações). Em todos os pontos de tempo, os valores médios da glicemia em 30 semanas foram mais baixos no grupo o qual fez uso de Lixisenatida + Insulina Glargina do que, tanto no grupo insulina glargina quanto no grupo lixisenatida, com uma única exceção do valor antes do café da manhã, que foi similar entre o grupo o qual fez uso de Lixisenatida + Insulina Glargina e o grupo que fez uso de insulina glargina.
Estudos clínicos em pacientes com diabetes tipo 2 não controlados com insulina basal
Em substituição à insulina basal
Um total de 736 pacientes com diabetes tipo 2 participou de um estudo randomizado, de 30 semanas, controlado com ativo, aberto, com 2 braços de tratamento, grupos paralelos, multicêntrico, para avaliar a eficácia e segurança de Lixisenatida + Insulina Glargina em comparação à insulina glargina (100 unidades/mL).
Os pacientes triados que apresentavam diabetes tipo 2 foram tratados com insulina basal por pelo menos 6 meses, recebendo uma dose diária estável entre 15 e 40 unidades isoladamente ou em combinação com 1 ou 2 antidiabéticos orais (metformina ou uma sulfonilureia ou uma glinida ou um inibidor de SGLT-2 ou um inibidor de DPP-4), que apresentavam HbA1c entre 7,5% e 10% e glicemia em jejum inferior ou igual a 180 mg/dL [9,99 mmol/L] ou 200 mg/dL [11,1 mmol/L] dependendo do tratamento antidiabético prévio do paciente.
Após a triagem, os pacientes elegíveis (n=1.018) entraram em uma fase de tratamento (run-in) de 6 semanas, onde os pacientes permaneceram ou passaram por substituição para a insulina glargina, no caso deles utilizarem outra insulina basal, e tiveram a sua dose de insulina titulada/estabilizada enquanto continuaram com a metformina (se utilizada anteriormente). Quaisquer outros antidiabéticos orais foram descontinuados.
No final do período de tratamento (run-in), os pacientes com HbA1c entre 7 e 10%, glicemia em jejum ≤ 140 mg/dL [7,77 mmol/L] e dose diária de insulina glargina de 20 a 50 unidades, foram randomizados para Lixisenatida + Insulina Glargina (n=367) ou para insulina glargina (n=369).
A população com diabetes tipo 2 apresentava as seguintes características:
- Idade média de 60 anos;
- 46,7% do sexo masculino;
- 91,7% caucasiano;
- 5,2% negro ou afro-americano;
- 17,9% hispânico.
A média de IMC na triagem foi de aproximadamente 31 kg/m2.
A duração média da diabetes era de aproximadamente 12 anos.
Na Semana 30, Lixisenatida + Insulina Glargina proporcionou uma melhora estatisticamente significativa na HbA1c (valor p < 0,0001) em comparação à insulina glargina.
Tabela 3 – Resultados em 30 semanas - Estudo com diabetes tipo 2 não controlada com insulina basal (população mITT):
- | Lixisenatida + Insulina Glargina | Insulina glargina |
Número de indivíduos (mITT) | 366 | 365 |
HbA1c (%) | ||
Na triagem (média) | 8,5 | 8,5 |
Linha Basal (média;após tratamento run in) | 8,1 | 8,1 |
Final do Tratamento (média) | 6,9 | 7,5 |
Alteração LS basal (média) | -1,1 | -0,6 |
Diferença vs insulina glargina (média) [95% IC] (valor p) | -0,5 [-0,6, -0,4] (< 0,0001) | |
Pacientes [n (%)] atingindo HbA1c < 7% na Semana 30 | 201 (54,9%) | 108 (29,6%) |
Glicemia em jejum (mg/dL) (mmol/L) | ||
Linha Basal (Média) | 132,0 [7,33] | 132,0 [7,32] |
| Final do tratamento (Média) | 122,1 [6,78] | 120,5 [6,69] |
Alteração LS basal (média) | -6,3 [-0,35] | -8,3 [-0,47] |
Glicose de 2 horas pós-prandial (mg/dL) [mmol/L] [variação de glicose de 2 h* (mg/dL) {mmol/L}] | ||
Alteração LS basal por 30 semanas (média) | -85,1 [-4,72] [-70,2 {-3,90}] | -25,1 [-1,39] [-8,4 {-0,47}] |
Média de peso corporal (kg) | ||
| Linha Basal (média) | 87,8 | 87,1 |
Alteração LS basal (média) | -0,7 | 0,7 |
| Comparação vs insulina glargina [95% IC] (valor p) | -1,4 [-1,8 a -0,9] (< 0,0001) | |
Número de pacientes (%) atingindo HbA1c < 7,0% sem ganho de peso corporal na Semana 30 | 125 (34,2%) | 49 (13,4%) |
Diferença na proporção vs insulina glargina [95% IC] (valor p) | 20,8 [15,0 to 26,7] (< 0,0001) | |
Dose diária de insulina glargina | ||
Linha Basal (Média) | 35,0 | 35,2 |
Desfecho (média) | 46,7 | 46,7 |
Alteração LS na dose de insulina na Semana 30 (média) | 10,6 | 10,9 |
* Glicose de 2 h pós-prandial menos o valor da glicose pré-refeição.
Figura 2 – HbA1c média (%) no início da triagem, na randomização e em cada ponto de tempo (concluído) e na Semana 30 (LOCF*) - população mITT:
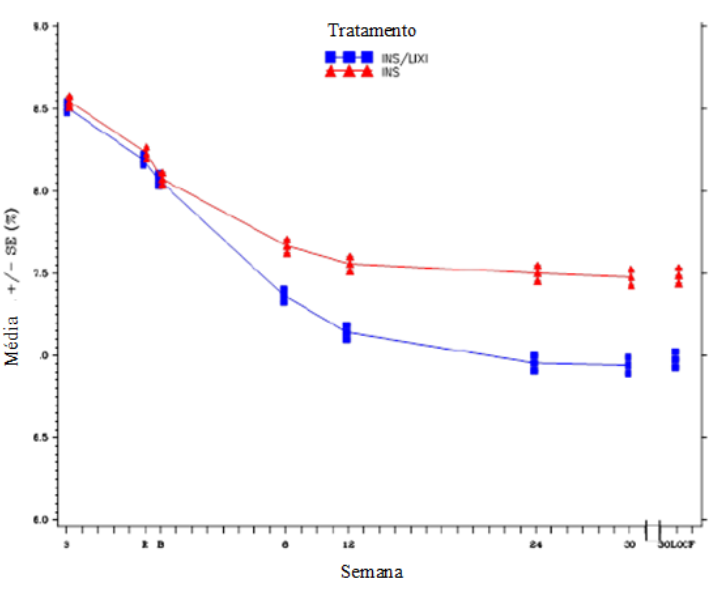
*LOCF = última observação realizada.
Resultados de Estudos Cardiovasculares
A segurança cardiovascular da insulina glargina e da lixisenatida foi estabelecida nos estudos clínicos Origin e Elixa, respectivamente. Nenhum resultado de estudo cardiovascular exclusivo foi realizado com Lixisenatida + Insulina Glargina.
Insulina glargina
O estudo Origin (Outcome Reduction with Initial Glargine Intervention - Desfecho da redução com intervenção inicial com glargina) foi um estudo aberto, randomizado, com 12.537 pacientes que comparou Lantus com o tratamento padrão no momento para a ocorrência de um evento cardiovascular adverso maior (Mace). Mace foi definido como a composição de morte cardiovascular, infarto não-fatal do miocárdio e acidente vascular cerebral não-fatal. A incidência de Mace foi semelhante entre Lantus e o tratamento padrão no estudo Origin [HR (95% IC) para Mace; 1,02 (0,94, 1,11)].
No estudo Origin, a incidência total de câncer (todos os tipos combinados) [Hazard Ratio (95% IC); 0,99 (0,88, 1,11)] ou morte por câncer [Hazard Ratio (95% IC); 0,94 (0,77, 1,15)] também foi semelhante entre os grupos de tratamento.
Lixisenatida
O estudo Elixa foi um estudo randomizado, duplo-cego, controlado por placebo, multinacional, que avaliou resultados cardiovasculares (CV) durante o tratamento com lixisenatida em pacientes (n=6068) com diabetes mellitus tipo 2 após uma recente síndrome coronária aguda. A composição do desfecho de eficácia primário foi o tempo para a primeira ocorrência de qualquer dos seguintes eventos declarados positivamente pelo Comitê de Adjudicação de Eventos Cardiovasculares: morte cardiovascular, infarto não-fatal do miocárdio, acidente vascular cerebral não-fatal, ou hospitalização por angina instável. Os desfechos secundários cardiovasculares incluíram a composição do desfecho primário, ou hospitalização por insuficiência cardíaca ou revascularização coronariana.
Mudanças na razão albumina/creatinina urinária em 108 semanas foi também um desfecho secundário pré-especificado.
A duração média do tratamento foi de 22,4 meses no grupo lixisenatida e 23,3 meses no grupo placebo, e a duração média do estudo de acompanhamento foi de 25,8 e 25,7 meses, respectivamente. A HbA1c média (± DP) nos grupos lixisenatida e placebo foi de 7,72 (± 1,32)% e 7,64 (± 1,28) % no início do tratamento e 7,46 (± 1,51)% e 7,61 (±1,48) % aos 24 meses, respectivamente.
A incidência do desfecho primário foi semelhante entre os grupos lixisenatida e placebo; o hazard ratio (HR) para lixisenatida versus placebo foi de 1,017, com um intervalo de confiança associado de 95% (IC) de 0,886 a 1,168.
Porcentagens semelhantes entre os tratamentos também foram observadas para os desfechos secundários e para todos os componentes individuais dos desfechos compostos. Os percentuais de pacientes hospitalizados por insuficiência cardíaca foram de 4,0% e 4,2% nos grupos lixisenatida e placebo, respectivamente (HR [IC 95%] = 0,96 [0,75-1,23]).
Foi observado um aumento menor na razão albumina/creatinina urinária do início do tratamento até a Semana 108 com lixisenatida em comparação ao placebo (-10,04% ± 3,53%; IC 95% = -16,95%, -3,13%).
Referências bibliográficas
1. Pfeiffer M.A., Claggett B., Diaz, R.D. et al. Lixisenatide in Patients with Type 2 Diabetes and Acute Coronary Syndrome. N Engl J Med 2015; 373: 2247-57.
2. The Origin Trial Investigators. Basal Insulin and Cardiovascular and Other Outcomes in Dysglycemia. N Engl J Med 2012; 367: 319-28.
3. Aroda V.R., Rosenstock J., Wysham C. et al. Efficacy and Safety of LixiLan, a Titratable Fixed-Ratio Combination of Insulin Glargine Plus Lixisenatide in Type 2 Diabetes Inadequately Controlled on Basal Insulin and Metformin: The LixiLan-L Randomized Trial. Diabetes Care 2016; 39: 1972–1980.
4. Rosenstock J., Aronson R., Grunberger G. et al. Benefits of LixiLan, a Titratable Fixed-Ratio Combination of Insulin Glargine Plus Lixisenatide, Versus Insulin Glargine and Lixisenatide Monocomponents in Type 2 Diabetes Inadequately Controlled With Oral Agents: The LixiLan-O Randomized Trial. Diabetes Care. 2016 Nov; 39(11): 2026-2035.
Características Farmacológicas
Mecanismo de ação
Lixisenatida + Insulina Glargina combina dois agentes anti hiperglicêmicos com mecanismos de ação complementares: insulina glargina, um análogo de insulina basal, e lixisenatida, um agonista do receptor de GLP-1, que tem como alvo a glicemia em jejum (FPG) e glicemia pós prandial (PPG) para melhorar o controle glicêmico em pacientes com diabetes tipo 2, enquanto minimiza o ganho de peso e o risco de hipoglicemia.
Insulina glargina
A atividade primária da insulina, incluindo a insulina glargina, consiste na regulação do metabolismo da glicose.
A insulina e os seus análogos diminuem a glicose no sangue, estimulando a captação da glicose periférica, especialmente pelo músculo esquelético e tecido adiposo, e através da inibição da produção de glicose hepática.
A insulina inibe a lipólise e proteólise, e aumenta a síntese de proteínas.
Lixisenatida
A lixisenatida é um agonista do receptor de peptídeo semelhante ao glucagon (GLP-1). O receptor GLP-1 é um alvo para o GLP-1 nativo, um hormônio endógeno com atividade incretina que potencializa a secreção de insulina glicose-dependente pelas células beta e suprime o glucagon de células alfa no pâncreas.
Semelhante ao GLP-1 endógeno, a ação de lixisenatida é mediada via interação especifica com os receptores GLP-1, incluindo aqueles em células alfa e beta pancreáticas.
Após uma refeição, a lixisenatida ativa as seguintes respostas fisiológicas individuais:
- Aumenta a secreção de insulina pelas células beta;
- Retarda o esvaziamento gástrico;
- Suprime a secreção de glucagon pelas células alfa.
A lixisenatida estimula a secreção de insulina dependente de glicose. Em paralelo, a secreção de glucagon é suprimida. A lixisenatida também retarda o esvaziamento gástrico reduzindo assim a taxa de glicose que aparece na circulação e é absorvida derivada da alimentação. A lixisenatida foi apresentada para preservar a função de células beta e prevenir a morte celular (apoptose) em células isoladas de ilhotas pancreáticas humanas.
Propriedades farmacodinâmicas
A combinação de insulina glargina e lixisenatida não apresenta impacto sobre a farmacodinâmica da insulina glargina. O impacto da combinação de insulina glargina e lixisenatida sobre a farmacodinâmica de lixisenatida não foi avaliado em estudos de fase 1.
Consistente com um perfil de concentração/tempo relativamente constante da insulina glargina ao longo de 24 horas com nenhum pico pronunciado quando administrado isoladamente, o perfil da taxa/tempo de utilização da glicose foi semelhante, nenhum pico pronunciado, quando administrado na combinação insulina glargina/lixisenatida.
O tempo de ação das insulinas, incluindo Lixisenatida + Insulina Glargina, pode variar entre indivíduos e no mesmo indivíduo.
Insulina glargina
Em estudos clínicos com insulina glargina (100 unidades/mL) o efeito de redução da glicose em uma base molar (isto é, quando administrados nas mesmas doses) de insulina glargina intravenosa é aproximadamente o mesmo que o descrito para a insulina humana.
Lixisenatida
Em um estudo controlado por placebo de 28 dias em pacientes com diabetes tipo 2 para avaliar os efeitos de doses de 5 a 20 mcg de lixisenatida, uma ou duas vezes ao dia, sobre a glicemia induzida por uma refeição padrão de café da manhã, 10 e 20 mcg uma ou duas vezes ao dia de lixisenatida melhorou o controle glicêmico através dos efeitos da diminuição das concentrações de glicose pós-prandial e em jejum em pacientes com diabetes tipo 2. A lixisenatida administrada neste estudo pela manhã na dose diária de 20 mcg manteve reduções estatisticamente significativas na glicemia pós-prandial após o café da manhã, almoço e jantar.
Glicemia pós-prandial
Em um estudo de tratamento de 4 semanas em pacientes com diabetes tipo 2, em combinação com metformina e em um estudo de tratamento de 8 semanas em combinação com insulina glargina com ou sem metformina, a lixisenatida 20 mcg uma vez ao dia administrada antes do café da manhã, demonstrou redução da glicemia pósprandial (AUC 0:30-4:30h) após um teste com refeição. O número de pacientes com níveis pós-prandiais de 2 h de glicose abaixo de 140 mg/dL (7,77 mmol/L) foi de 69,3% após 28 dias e 76,1% após 56 dias.
Secreção de insulina
Em um estudo em monoterapia, a lixisenatida isoladamente restaura a primeira fase de secreção de insulina em pacientes com diabetes tipo 2 de uma maneira dependente da glicose em 2,8 vezes (IC 90%, 2,5-3,1) e aumenta a secreção de insulina na segunda fase em 1,6 vezes (IC 90%, 1,4 1,7) em comparação ao placebo, como medido através da AUC.
Esvaziamento gástrico
Após um teste com refeição padronizada, a lixisenatida retarda o esvaziamento gástrico, diminuindo assim o ritmo de absorção da glicose pós-prandial. Após tratamento de 28 dias com lixisenatida isoladamente, o efeito do retardamento de esvaziamento gástrico é mantido em pacientes com diabetes tipo 2.
Secreção de glucagon
A lixisenatida 20 mcg uma vez ao dia isoladamente demonstrou diminuir os níveis de glucagon pós-prandial versus o basal após um teste com refeição em pacientes com diabetes tipo 2. Em um estudo hipoglicêmico controlado por placebo com indivíduos saudáveis avaliando o efeito de uma única injeção de 20 mcg de lixisenatida na resposta ao glucagon, a resposta contrarreguladora do glucagon foi preservada sob condições de hipoglicemia, na presença de concentrações plasmáticas de lixisenatida eficazes.
Eletrofisiologia cardíaca (QTc)
O efeito de lixisenatida na repolarização cardíaca foi testado em um estudo QTc (1,5 vez a dose de manutenção aprovada) o qual não indicou nenhum impacto relevante de lixisenatida na repolarização ventricular.
Frequência cardíaca
Nenhum aumento na frequência cardíaca média foi observado com Lixisenatida + Insulina Glargina em estudos de fase 3 controlados por placebo.
Propriedades farmacocinéticas
A relação insulina glargina/lixisenatida não apresenta impacto relevante sobre a farmacocinética da insulina glargina em Lixisenatida + Insulina Glargina.
Em comparação à administração de lixisenatida isoladamente, a Cmáx é menor enquanto a AUC é geralmente comparável quando administrada como Lixisenatida + Insulina Glargina. As diferenças observadas na farmacocinética da lixisenatida quando administrada como Lixisenatida + Insulina Glargina ou isoladamente não são consideradas clinicamente relevantes.
Absorção
Após a administração subcutânea da combinação de insulina glargina/lixisenatida em pacientes com diabetes tipo 1, a insulina glargina não mostrou pico pronunciado. A exposição à insulina glargina variou de 86%a 101% em comparação à administração de insulina glargina isoladamente.
Após a administração subcutânea da combinação de insulina glargina/lixisenatida em pacientes com diabetes tipo 1, o tmáx médio da lixisenatida variou de 2,5 a 3,0 horas. Houve uma pequena diminuição na Cmáx da lixisenatida de 22-34% em comparação à administração simultânea separada de insulina glargina e lixisenatida, o que não é provável que seja clinicamente significativa.
Não há diferenças clinicamente significativas na taxa de absorção quando a lixisenatida é administrada por via subcutânea no abdome, coxa ou braço.
Distribuição
Lixisenatida:
A lixisenatida apresenta um nível moderado de ligação (55%) às proteínas humanas.
Metabolismo e Eliminação
Insulina glargina:
Um estudo de metabolismo em seres humanos que receberam insulina glargina isoladamente indicou que a insulina glargina é parcialmente metabolizada no terminal carboxílico da cadeia B no depósito subcutâneo para formar dois metabólitos ativos com uma atividade in vitro semelhante à da insulina humana, M1 (21A-Gliinsulina) e M2 (21A-Gli-des-30B- Tir insulina). O fármaco inalterado e os produtos de degradação também estão presentes na circulação.
Lixisenatida:
Como um peptídeo, a lixisenatida é eliminada através da filtração glomerular, seguida por reabsorção tubular e subsequente degradação metabólica, resultando em peptídeos menores e aminoácidos, os quais são reintroduzidos no metabolismo proteico.
Populações especiais
Idade, Raça e Sexo (insulina glargina):
Insulina glargina | Lixisenatida |
O efeito da idade, raça e sexo na farmacocinética da insulina glargina não foi avaliado. Em estudos clínicos controlados em adultos com insulina glargina (100 unidades/mL), análises de subgrupo baseadas na idade, raça e sexo não mostraram diferenças na segurança e eficácia | Com base na análise farmacocinética populacional, idade, peso corporal, sexo e raça não apresentam efeitos clinicamente significativos na farmacocinética de lixisenatida |
Obesidade:
O efeito do Índice de Massa Corporal (IMC) na farmacocinética de Lixisenatida + Insulina Glargina não foi avaliado.
Insuficiência renal:
Um estudo de dose única, aberto avaliou a farmacocinética de lixisenatida 5 mcg em indivíduos com diferentes graus de insuficiência renal (classificados utilizando a fórmula de Cockcroft-Gault para a depuração da creatinina (CLcr)) em comparação com indivíduos saudáveis.
Não houve diferenças relevantes na Cmáx e AUC médias de lixisenatida entre indivíduos com função renal normal e em indivíduos com insuficiência renal leve (CLcr 60-90 mL/min). Em indivíduos com insuficiência renal moderada (CLcr 30-60 mL/min) a AUC foi aumentada em cerca de 51% e em indivíduos com insuficiência renal grave (CLcr 15-30 mL/min) a AUC foi aumentada em aproximadamente 87%.
Insuficiência hepática (lixisenatida):
Uma vez que a lixisenatida é eliminada principalmente pelo rim, nenhum estudo farmacocinético foi realizado em pacientes com insuficiência hepática aguda ou crônica. Não é esperado que a disfunção hepática afete a farmacocinética de lixisenatida.
Dados de segurança pré-clínicos:
Não foram realizados estudos em animais com insulina glargina e lixisenatida combinadas para avaliar carcinogênese, mutagênese e insuficiência da fertilidade.
Insulina glargina | Lixisenatida |
Os dados pré-clínicos para a insulina glargina não revelam riscos especiais para o ser humano, segundo estudos convencionais de farmacologia de segurança, toxicidade de dose repetida, genotoxicidade, potencial carcinogênico e toxicidade reprodutiva | Em um estudo de carcinogenicidade subcutânea de dois anos de duração, tumores de tireoide de células C não letais foram observados em ratos e camundongos e são considerados como sendo causados por um mecanismo GLP-1 não genotóxico mediado por receptor ao qual os roedores são particularmente sensíveis. Hiperplasia de células C e adenoma foram observados em todas as doses em ratos e nenhum efeito adverso de nível (NOEL) pôde ser definido. Em camundongos, estes efeitos ocorreram em razão de exposição acima de 9,3 vezes quando comparado com a exposição humana na dose terapêutica. Nenhum carcinoma de célula C foi observado em camundongos e, ocorreu carcinoma de células C em ratos na razão relativa de exposição a uma dose terapêutica de exposição humana de cerca de 900 vezes. Estudos em animais não indicam quaisquer efeitos prejudiciais diretos em relação à fertilidade em ratos machos e fêmeas. Lesões testiculares e do epidídimo reversíveis foram observadas em cães tratados com lixisenatida. Nenhum efeito relacionado à espermatogênese foi observado em homens saudáveis. Em estudos de desenvolvimento embriofetal, foram observadas malformações, retardo no crescimento, retardo de ossificação e efeitos esqueléticos em ratos em todas as doses (5 vezes a taxa de exposição em comparação à exposição humana) e em coelho com doses elevadas (32 vezes a taxa de exposição em comparação à exposição humana) de lixisenatida. Em ambas as espécies, houve uma toxicidade materna ligeira consistindo de baixo consumo de alimentos e redução do peso corporal. O crescimento neonatal foi reduzido em ratos machos expostos a elevadas doses de lixisenatida durante a gestação e lactação tardia, com um ligeiro aumento da mortalidade da prole observada |

 Revisado por Isabelle Baião de Mello Neto (CRF-MG 24309)
Revisado por Isabelle Baião de Mello Neto (CRF-MG 24309)