Qual a ação da substância do Libtayo?
Resultados de Eficácia
A eficácia e segurança de Cemiplimabe em pacientes com carcinoma cutâneo de células escamosas (também denominado Carcinoma Espinocelular - CEC) metastático (nodal ou distante) ou carcinoma cutâneo de células escamosas (CEC) localmente avançado que não eram candidatos a cirurgia foram estudadas em um estudo clínico prospectivos, Estudo 1540. O estudo 1540 foi um estudo fase II, multicêntrico, aberto que incluiu 193 pacientes com CEC metastático ou CEC localmente avançado no momento do corte de dados em 30 de junho de 2018, com um tempo médio de acompanhamento de 7,4 meses.
Dados de eficácia de suporte foram obtidos em um estudo fase I, multicêntrico, aberto (Estudo 1423) em pacientes com tumores sólidos, dentre os quais os pacientes com CEC (n = 26) que se enquadraram na definição de CEC avançado utilizado no estudo pivotal (corte de dados em 30 de junho de 2018). Com uma duração média de acompanhamento de 13,3 meses (intervalo: 1,1-21,0 meses), a taxa de resposta objetiva (TRO) confirmada por revisão central independente foi de 50% (13 respostas de 26 pacientes) e o Intervalo de Confiança de 95% foi de 29,9-70,1%. A duração mediana estimada da resposta foi de 20,3 meses e a variação observada foi de 1,0 a 20,3 meses. A duração da resposta foi ≥ 6 meses para 84,6% dos pacientes (11 dos 13 respondedores).
Ambos os estudos excluíram pacientes com doença autoimune que necessitaram de terapia sistêmica com agentes imunossupressores dentro de 5 anos; história de transplante de órgão sólido; história de pneumotite dentro de 5 anos, tratamento prévio com anti-PD-1 / PD-L1 ou outra terapia inibidora de checkpoints imunológicos; infecção por HIV, hepatite B ou hepatite C; metástase cerebral ou escore de desempenho ECOG ≥ 2.
No Estudo 1540, os pacientes receberam Cemiplimabe até progressão inequívoca da doença, toxicidade inaceitável ou conclusão do tratamento planejado (3 mg/kg a cada 2 semanas durante 96 semanas ou 350 mg a cada 3 semanas durante 54 semanas). Os pacientes poderiam continuar o tratamento além da progressão inicial, a critério do investigador. Se os pacientes com doença localmente avançada apresentassem resposta suficiente ao tratamento, a cirurgia com intenção curativa era permitida. As avaliações da resposta tumoral foram realizadas a cada 8 ou 9 semanas (para pacientes que receberam 3 mg/kg a cada 2 semanas ou 350 mg a cada 3 semanas, respectivamente). O desfecho primário do Estudo 1540 foi confirmado - taxa de resposta objetiva (TRO), conforme avaliado por revisão central independente (RCI). Para pacientes com CEC metastático sem lesões alvo visíveis externamente, a TRO foi determinada pelos Critérios de Avaliação de Resposta em Tumores Sólidos (RECIST 1.1). Para pacientes com lesões alvo externamente visíveis (CEC localmente avançado e CEC metastático), a TRO foi determinada por um endpoint composto que integrou as avaliações de RCI de dados radiológicos (RECIST 1.1) e fotografia médica digital (critérios da OMS). O desfecho secundário principal foi a duração da resposta (DR). Outros desfechos secundários foram sobrevida livre de progressão (SLP), sobrevida global (SG), taxa de resposta completa (TRC) e mudança nas pontuações nos resultados relatados pelos pacientes no Questionário de Qualidade de Vida da Organização Europeia de Pesquisa e Tratamento do Câncer (EORTC).
Os resultados são apresentados dos 167 pacientes do Estudo 1540. Destes 167 pacientes, 103 eram CEC metastático e 64 eram CEC localmente avançado com uma idade média de 72 anos (variação: 38 a 96). Sessenta e cinco (38,9%) pacientes tinham 75 anos ou mais, 60 pacientes (35,9%) tinham de 65 a menos de 75 anos, e 42 pacientes (25,1%) tinham menos de 65 anos. Um total de 139 (83,2%) pacientes eram do sexo masculino e 162 (97%) eram brancos; o escore de desempenho do ECOG foi 0 (46,1%) ou 1 (53,9%). Trinta e seis e meio por cento (36,5%) dos pacientes havia recebido pelo menos uma terapia sistêmica anticâncer anterior, 91% dos pacientes haviam recebido cirurgia prévia relacionada ao câncer e 69,5% dos pacientes haviam recebido radioterapia prévia. Entre os pacientes com CEC metastático, 75,7% tinham metástases à distância e 23,3% tinham apenas metástases nodais.
Os resultados de eficácia do Estudo 1540 estão apresentados na Tabela 1 e Figura 1.
Tabela 1: Resultados de eficácia (Estudo 1540) - CEC metastático, CEC localmente avançado e CEC combinado.
Desfechos de Eficáciaa | CEC metastático (N = 103) | CEC localmente avançado (N = 64) | CEC combinado (N = 167) |
Taxa de Resposta Objetiva Confirmada (TRO) | |||
TRO % | 44,7% (34,9; 54,8) | 45,3% (32,8; 58,3) | 44,9% |
Taxa de Resposta Completa (TRC) b | 8,7% | 10,9% | 9,6% |
Taxa de Resposta Parcial (TRP) | 35,9% | 34,4% | 35,3% |
Duração da Resposta (DR) c | |||
Média (meses) | NA | NA | NA |
Variação (meses) | 2,1 – 20,7+ | 1.9 – 22.4+ | 1.9 – 22.4+ |
Pacientes com DR ≥ 6 meses, % | 69,6% | 62,1% | 66,7% |
Tempo de Resposta (meses) | |||
Média | 2,0 (1,7; 9,1) | 2,1 (1,8; 8,8) | 2,0 |
Taxa de Controle de Duração de Doenças (TCDD) em 16 semanas | |||
TCDD % | 59,2% (49,1; 68,8) | 59,4% (46,4;71,5) | 59,3% |
IC: intervalo de confiança; NA: não alcançado.
+: indica em andamento na última avaliação com 3 ou mais avaliações.
a Inclui apenas pacientes com cicatrização completa do comprometimento cutâneo prévio; pacientes com CEC localmente avançado no Estudo 1540 necessitaram de biópsia para confirmar a resposta completa.
b Nos grupos metastático e localmente avançado, a duração média de acompanhamento foi de 9,0 e 8,8 meses, respectivamente.
Figura 1: Alteração percentual da lesão alvo da linha de base*
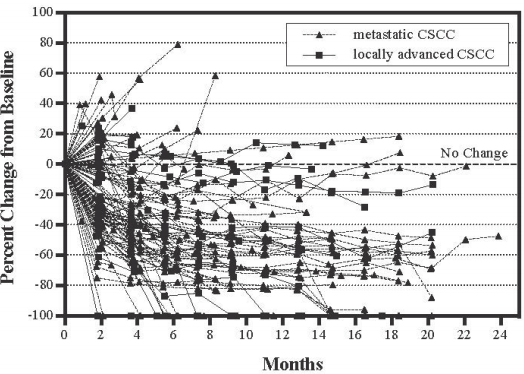
* Baseado nos critérios RECIST 1.1 ou OMS, cada linha representa a mudança individual do paciente na lesão alvo em 87 dos 108 pacientes que tiveram pelo menos uma avaliação tumoral avaliável.
Características Farmacológicas
Propriedades farmacodinâmicas
Agente antineoplásico. Anticorpo monoclonal.
O Cemiplimabe é um anticorpo monoclonal recombinante humano imunoglobulina G4 (IgG4) que se liga à PD-1 e bloqueia sua interação com PD-L1 e PD-L2, contrariando a inibição mediada pela PD-1 da resposta imune, incluindo a resposta imune antitumoral. Em modelos de tumor de ratos singênicos o bloqueio da atividade de PD-1 resultou na diminuição do crescimento do tumor.
A ligação de PD-L1 e PD-L2, à PD-1 nas células T, inibe a proliferação de células T e a produção de citocinas. Esta via pode contribuir para a inibição da vigilância imune ativa das células T dos tumores.
O Cemiplimabe é produzido por tecnologia de DNA recombinante em cultura de suspensão de células de ovário de hamster chinês (CHO).
A maioria dos pacientes que recebeu Cemiplimabe teve redução das lesões alvo, com relação ao valor basal de 20 a 100%.
Propriedades farmacocinéticas
As concentrações de Cemiplimabe foram coletados em 505 pacientes com vários tumores sólidos, incluindo 135 pacientes com CEC (carcinoma espinocelular), que receberam o Cemiplimabe. Com base no mecanismo de ação descrito e na ligação ao checkpoint (PD-1), seria de se esperar uma cinética não linear do Cemiplimabe mediada pelo alvo. Nos regimes de dosagem de 1 mg/kg a 10mg/kg a cada 2 semanas e incluindo 350 mg a cada 3 semanas, a farmacocinética do Cemiplimabe foi linear e proporcional à dose, sugerindo saturação da via mediada pelo alvo durante o intervalo de dosagem.
A exposição semelhante de Cemiplimabe no soro é alcançada com as doses de 350 mg a cada 3 semanas e 3 mg / kg a cada 2 semanas. Com 350 mg a cada 3 semanas, os valores da concentração mediana em estado estacionário do Cemiplimabe variou entre Cmáx de 166 mg/L e um desvio de 59 mg/L. A exposição no estado estacionário é alcançada após aproximadamente 4 meses de tratamento.
Distribuição
O Cemiplimabe é distribuído principalmente no sistema vascular com um volume de distribuição no estado estacionário de 5,2 L.
Eliminação
A depuração do Cemiplimabe é linear nas doses de 1 mg/kg a 10 mg/kg a cada duas semanas. A depuração de Cemiplimabe após a primeira dose é de aproximadamente 0,33L/dia. A depuração total de Cemiplimabe parece diminuir em aproximadamente 35% ao longo do tempo, resultando em uma depuração estacionária (CLSS) de 0,21L/dia; a diminuição do CL não é considerada clinicamente relevante. A meia-vida do intervalo de dosagem no estado estacionário é de 19,2 dias.
Populações especiais
Uma análise farmacocinética populacional sugere que os seguintes fatores não têm efeito clinicamente significativo na exposição do Cemiplimabe: idade, sexo, peso corporal, raça, tipo de câncer, carga tumoral, nível de albumina, insuficiência hepática leve e comprometimento renal.
Uso geriátrico
Dos 219 pacientes com CEC metastático e CEC localmente avançado tratados com Cemiplimabe, 25,1% (55/219) tinham menos de 65 anos, 34,2% (75/219) tinham de 65 a menos de 75 anos e 40,6% (89/219) tinham 75 anos. As incidências de eventos adversos totais foram geralmente consistentes em todos os grupos etários.
Nos 167 pacientes avaliados para eficácia, a taxa de resposta objetiva (95% IC) foi de 42,9% (27,7%, 59%) em pacientes com menos de 65 anos, 48,3% (35,2%, 61,6%) em pacientes que tinham de 65 a menos de 75 anos, e 43,1% (30,8%, 56,0%) em pacientes com 75 anos ou mais.
Insuficiência renal
O efeito do comprometimento renal sobre a exposição de Cemiplimabe foi avaliado por uma análise farmacocinética populacional em doentes com insuficiência renal leve (CLcr 60 a 89 ml / min; n = 177), moderada (CLcr 30 a <60 ml / min; n = 83), ou severa (CLcr <30 mL / min; n = 4). Não foram encontradas diferenças clinicamente importantes na exposição de Cemiplimabe entre pacientes com insuficiência renal e pacientes com função renal normal.
Insuficiência hepática
O efeito do comprometimento hepático na exposição de Cemiplimabe foi avaliado pela análise farmacocinética populacional em doentes (n = 5) com insuficiência hepática leve (bilirrubina total [BT] superior a 1,0 a 1,5 vezes o limite superior normal [LSN] e qualquer AST); não foram encontradas diferenças clinicamente importantes na exposição de Cemiplimabe entre pacientes com insuficiência hepática leve e pacientes com função hepática normal. Cemiplimabe não foi estudado em doentes com insuficiência hepática moderada ou severa.
Dados de segurança pré-clínica
Toxicologia Animal e / ou Farmacologia
A segurança do Cemiplimabe foi avaliada em estudos de toxicidade de dose repetida de 1 mês e 6 meses em macacos cynomolgus. O nível de efeito adverso não observado (NOAEL) foi a dose mais elevada administrada nestes estudos (50 mg / kg / semana).
Em modelos animais, a inibição da sinalização PD-L1/PD-1 aumentou a severidade de algumas infecções e aumentou as respostas inflamatórias. Camundongos knockout de PD-1 infectados com M. tuberculosis exibiram acentuada diminuição da sobrevida em comparação com controles do tipo selvagem, que se correlacionaram com o aumento da proliferação bacteriana e respostas inflamatórias nestes animais. Camundongos e camundongos knockout para PD-L1 e PD-1 que receberam anticorpo bloqueador de PD-L1 também mostraram diminuição da sobrevida após infecção pelo vírus da coriomeningite linfocítica.
Carcinogênese, mutagênese, prejuízo da fertilidade
Nenhum estudo foi realizado para testar o potencial do Cemiplimabe quanto à carcinogenicidade ou genotoxicidade. Em um estudo de avaliação de fertilidade de dose repetida de 3 meses com macacos cynomolgus sexualmente maduros na dose mais elevada testada (50 mg / kg / semana), não foram observados efeitos relacionados com o Cemiplimabe nos parâmetros de avaliação da fertilidade (ciclo menstrual, análise de sémen ou medidas testiculares) ou em órgãos reprodutivos masculinos ou femininos.
Teratogenicidade
Estudos de reprodução animal não foram realizados com o Cemiplimabe.

 Revisado por Isabelle Baião de Mello Neto (CRF-MG 24309)
Revisado por Isabelle Baião de Mello Neto (CRF-MG 24309)