Quais as reações adversas e os efeitos colaterais do IVB Insulina Humana R?
As frequências são definidas como:
- Reações adversas muito frequentes (ocorrem em mais de 10% dos pacientes que utilizam este medicamento), frequentes (ocorrem entre 1% e 10% dos pacientes que utilizam este medicamento), pouco frequentes (ocorrem entre 0,1% e 1% dos pacientes que tomam este medicamento), raras (ocorrem em 0,01% a 0,1% dos pacientes que utilizam este medicamento), muito raras (ocorrem em menos de 0,01% dos pacientes que utilizam este medicamento), desconhecidas (não se pode calcular a partir dos dados disponíveis).
Experiência em estudos clínicos
Devido aos estudos clínicos terem sido conduzidos sob condições amplamente variáveis, a incidência de reações adversas relatadas nos estudos clínicos do medicamento pode não diretamente comparável à incidência relatada em estudos clínicos de outros medicamentos e pode não refletir a incidência observada na prática.
Os dados descritos abaixo refletem a exposição de 3017 pacientes ao Insulina Humana e incluem 1026 pacientes com diabetes tipo 1 e 1991 pacientes com diabetes tipo 2. A duração média de exposição foi de 8,17 meses para a população em geral, 8,16 meses e 8,18 meses para pacientes com diabetes tipo 1 e tipo 2, respectivamente. Na população geral, 1874 foram expostos ao Insulina Humana por 6 meses e 724 por mais de 1 ano. 620 e 1254 pacientes com diabetes tipo 1 e tipo 2, respectivamente, foram expostos ao Insulina Humana por até 6 meses. 238 e 486 pacientes com diabetes tipo 1 e tipo 2, respectivamente, foram expostos ao Insulina Humana por mais de um ano (exposição média = 1,8 anos). Insulina Humana foi estudado em estudos controlados com placebo e estudos ativamente controlados (n=3 e n=10, respectivamente).
A idade média da população foi 50,2 anos e 20 pacientes tinham mais que 75 anos de idade. 50,8% da população eram homens (sexo masculino); 82,6% eram brancos, 1,8% asiáticos, 4,9% negros ou afro-americanos e 9,7% hispânicos. Na linha basal, a população com diabetes tipo 1 tinha diabetes por uma média de 16,6 anos e HbA1c de 8,3% e a população com diabetes tipo 2 tinha diabetes por uma média de 10,7 anos e HbA1c de 8,8%. Na linha basal, 33,4% da população relataram neuropatia periférica, 32,0% relataram retinopatia e 19,6% tinham histórico de doença cardiovascular.
A Tabela 4 abaixo mostra reações adversas, excluindo hipoglicemia, associada com o uso de Insulina Humana no grupo de estudos clínicos controlados em pacientes com diabetes tipo 2. Estas reações adversas não estavam presentes na linha de base, elas ocorreram mais comumente no grupo Insulina Humana do que no grupo placebo e/ou comparador e em pelo menos 2% dos pacientes tratados com Insulina Humana.
Tabela 4. Reações adversas em pacientes com diabetes mellitus tipo 2 (excluindo hipoglicemia) tratados com Insulina Humana
| - | Placebo* (n = 290) | Insulina Humana (n = 1991) | Comparadores não placebo |
Tosse | 19,7% (muito comum) | 25,6% (muito comum) | 5,4% (comum) |
Dor ou irritação na garganta | 3,8% (comum) | 4,4% (comum) | 0,9% (incomum) |
Diminuição da Função Pulmonar | 0,0% (muito raro) | 0,9% (incomum) | 1,0% (incomum) |
Cefaléia | 2,8% (comum) | 3,1% (comum) | 1,8% (comum) |
Diarréia | 1,4% (comum) | 2,7% (comum) | 2,2% (comum) |
Tosse produtiva | 1,0% (incomum) | 2,2% (comum) | 0,9% (incomum) |
Fadiga | 0,7% (incomum) | 2,0% (comum) | 0,6% (incomum) |
Náusea | 0,3% (incomum) | 2,0% (comum) | 1,0% (incomum) |
Hipersensibilidade | 0,9% (incomum) | 0,8% (incomum) | 0,3% (incomum) |
*Partícula carreadora sem insulina foi usada como placebo.
A Tabela 5 mostra reações adversas, excluindo hipoglicemia, associadas com o uso de Insulina Humana no grupo de estudos clínicos controlados ativamente em pacientes com diabetes tipo 1. Estas reações adversas não estavam presentes na linha de base, elas ocorreram mais comumente no grupo Insulina Humana do que no comparador e em pelo menos 2% dos pacientes tratados com Insulina Humana.
Tabela 5. Reações adversas em pacientes com diabetes mellitus tipo 1 (excluindo hipoglicemia) tratados com Insulina Humana
| - | Insulina subcutânea (n = 835) | Insulina Humana |
Tosse | 4,9% (comum) | 29,4% (muito comum) |
Dor ou irritação na garganta | 1,9% (comum) | 5,5% (comum) |
Cefaléia | 2,8% (comum) | 4,7% (comum) |
Decréscimo no teste de função pulmonar | 1,0% (incomum) | 2,8% (comum) |
Bronquite | 2,0% (comum) | 2,5% (comum) |
Infecção no trato urinário | 1,9% (comum) | 2,3% (comum) |
Hipersensibilidade | 0,8% (incomum) | 0,6% (incomum) |
Hipoglicemia
Hipoglicemia é a reação adversa mais comum observada em pacientes usando insulina, incluindo Insulina Humana. A incidência de hipoglicemia severa e não severa de Insulina Humana versus placebo em pacientes com diabetes tipo 2 é mostrada na Tabela 6. Um evento hipoglicêmico foi registrado se o paciente relatou sintomas de hipoglicemia com ou sem um valor de glicose sanguínea consistente com hipoglicemia. Hipoglicemia severa foi definida como um evento com sintomas consistentes com hipoglicemia requerendo assistência de outra pessoa e associado com valor de glicemia consistente com hipoglicemia ou com recuperação imediata após tratamento para hipoglicemia.
Tabela 6. Incidência de hipoglicemia severa e não severa em estudo controlado por placebo em pacientes com diabetes tipo 2
| - | Placebo (N=176) | Insulina Humana | |
Hipoglicemia não severa | 30% | 67% | |
Hipoglicemia severa | 1,7% | 5,1% | |
Tosse
Aproximadamente 27% dos pacientes tratados com Insulina Humana relataram tosse (muito comum), comparado a aproximadamente 5,2% de pacientes tratados com comparador (comum). Em estudos clínicos, tosse foi a razão mais comum para descontinuação da terapia com Insulina Humana (2,8% dos pacientes tratados com Insulina Humana).
Declínio da Função Pulmonar
Em estudos clínicos durando até 2 anos, excluindo pacientes com doença crônica pulmonar, pacientes tratados com Insulina Humana tiveram um declínio 40 mL maior (95% CI: -80, -1), que o declínio da linha basal no volume expiratório forçado em um segundo (VEF1) comparado a pacientes tratados com tratamentos comparadores antidiabetes. O declínio ocorreu durante os primeiros 3 meses de terapia e persistiu ao longo de 2 anos (Figura 3). Um declínio no VEF1 de ≥ 15% ocorreu em 6% dos sujeitos tratados com Insulina Humana (comum) comparado com 3% dos sujeitos tratados com comparador (comum).
Figura 3. Mudança média (+/-EP) no VEF1 (litros) da linha basal para pacientes com diabetes tipo 1 e tipo 2
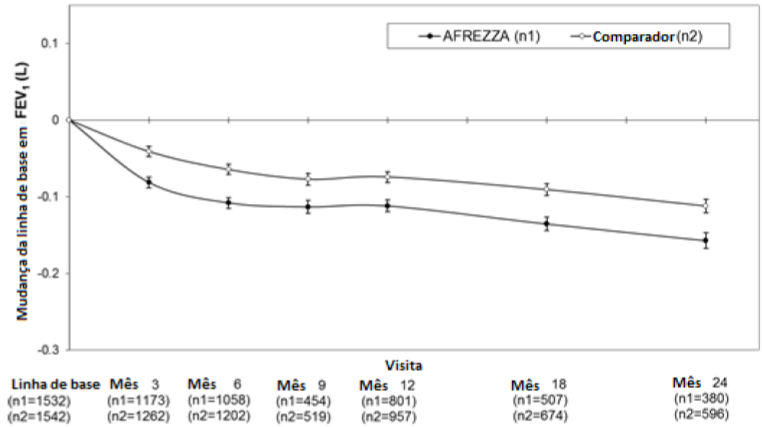
Ganho de peso
Ganho de peso pode ocorrer com algumas terapias baseadas em insulina, incluindo Insulina Humana, com frequência desconhecida. O ganho de peso foi atribuído aos efeitos anabólicos da insulina e diminuição da glicosúria. Em um estudo clínico com pacientes diabéticos tipo 2 houve uma média de ganho de peso de 0,49 kg dentre os pacientes tratados com Insulina Humana comparados com uma média de perda de peso de 1,13 kg dentre pacientes tratados com placebo.
Produção de anticorpos
Aumentos na concentração de anticorpos anti-insulina foram observados em pacientes tratados com Insulina Humana. Aumentos nos anticorpos anti-insulina são observados mais frequentemente com Insulina Humana do que com insulinas prandiais injetadas subcutaneamente. Pareceu haver um aumento médio menor de anticorpos anti-insulina em indivíduos que tomavam Insulina Humana e tinham <65 anos de idade, de um grupo racial não-caucasiano, e indivíduos na Europa Ocidental, enquanto os valores médios não mudaram muito. Os números em cada um desses subgrupos são pequenos e vários indivíduos com altos níveis de anticorpos anti-insulina distorcem os valores médios para cima, tornando difíceis as conclusões estatísticas válidas relacionadas às diferenças. A presença de anticorpos não se correlacionou com eficácia reduzida, como medido por HbA1c e glicose plasmática em jejum, ou reações adversas específicas.
Experiência pós-comercialização
As reações adversas a seguir foram identificadas durante o uso pós-aprovação de Insulina Humana. Como essas reações são relatadas voluntariamente por uma população de tamanho incerto, nem sempre é possível estimar com segurança sua frequência ou estabelecer uma relação causal com a exposição ao medicamento: broncoespasmo.
Atenção: este produto é um medicamento novo e, embora as pesquisas tenham indicado eficácia e segurança aceitáveis, mesmo que indicado e utilizado corretamente, podem ocorrer eventos adversos imprevisíveis ou desconhecidos. Nesse caso, notifique ao Sistema de Notificação de Eventos Adversos a Medicamentos – VIGIMED, disponível em http://portal.anvisa.gov.br/vigimed, ou para a Vigilância Sanitária Estadual ou Municipal.

 Revisado por Isabelle Baião de Mello Neto (CRF-MG 24309)
Revisado por Isabelle Baião de Mello Neto (CRF-MG 24309)