Qual a ação da substância do Tepezza?
Resultados de Eficácia
Teprotumumabe foi avaliado em 2 estudos randomizados, duplo cegos e controlado por placebo incluindo um total de 171 pacientes com Doença Ocular da Tireoide: Estudo 1 (NCT01868997) e Estudo 2 (NCT03298867). Os pacientes foram randomizados para receber teprotumumabe ou placebo em uma razão de 1:1. Os pacientes receberam infusões intravenosas (10 mg/kg para a primeira infusão e 20 mg/kg para as 7 infusões restantes) a cada 3 semanas para um total de 8 infusões. Os pacientes apresentavam diagnóstico clínico de Doença Ocular da Tireoide com sintomas e eram eutireoidianos, ou apresentavam níveis de tiroxina e triiodotironina livre menores que 50%, acima ou abaixo dos limites normais. Os critérios de entrada nos dois estudos duplo cegos de teprotumumabe delimitaram um CAS ≥4 para o olho mais gravemente afetado para inclusão e randomização; e qualquer sujeito cujo CAS diminuiu 2 ou mais pontos desde a triagem até a linha de base não foi eleito para randomização. Não mais de 9 meses deveriam ter decorrido entre o início dos sintomas da Doença Ocular da Tireoide ativa e a inclusão em ambos os estudos duplo-cegos. O tratamento cirúrgico prévio para a Doença Ocular da Tireoide não era permitido. A proptose variou de 16 a 33 mm e 125 pacientes (73%) apresentavam diplopia na avaliação inicial. Os sujeitos diabéticos deveriam ter a doença bem controlada e estável para serem incluídos nos estudos. Irradiação orbital prévia e neuropatia óptica foram considerados critérios de exclusão para ambos os estudos.
Um total de 84 pacientes foram randomizados para teprotumumabe e 87 pacientes foram randomizados para placebo. A idade mediana foi 52 anos (intervalo de 20 a 79 anos), 86% eram brancos, 9% eram negros ou afro-americanos, 4% eram asiáticos e 1% foi identificado como outro. A maioria (73%) era do sexo feminino. Na avaliação inicial, 27% dos pacientes eram fumantes.
A taxa de respondedores de proptose na semana 24 foi definida como a porcentagem de pacientes com redução ≥2 mm na proptose no olho em estudo desde a avaliação inicial, sem deterioração no olho não em estudo (aumento ≥2 mm) na proptose. Avaliações adicionais incluíram sinais e sintomas de Doença Ocular da Tireoide, incluindo dor, dor orbital provocada pelo olhar, inchaço, eritema da pálpebra, vermelhidão, quemose, inflamação, pontuação de atividade clínica e avaliações da visão funcional e aparência do paciente. Os resultados para proptose são apresentados na Tabela 1.
Tabela 1. Resultados de eficácia em pacientes com Doença Ocular daTireoide nos Estudos 1 e 2
| Estudo 1 | Estudo 2 | |||||
| Teprotumumabe (N=42) | Placebo (N=45) | Diferença (IC de 95%) | Teprotumumabe (N=41) | Placebo (N=42) | Diferença (IC de 95%) | |
| Taxa de respondedor de proptose na semana 24, % (n)¹ | 71% (30) | 20% (9) | 51% (33, 69) | 83% (34) | 10% (4) | 73% (59, 88) |
| Alteração média na proptose (mm) desde a avaliação inicial até a semana 24, média LS (SE)² | -2,5 (0,2) | -0,2 (0,2) | -2,3 (-2,8, - 1,8) | -2,8 (0,2) | -0,5 (0,2) | -2,3 (-2,8, - 1,8) |
¹ A diferença e o Intervalo de Confiança (IC) de 95% correspondente são baseados em uma média ponderada da diferença dentro de cada estrato de randomização (usuário de tabaco, sem uso de tabaco) usando as ponderações de CMH.
² Os resultados foram obtidos de um MMRM com uma matriz de covariância não estruturada e incluindo como efeitos fixos tratamento, estado de tabagismo, valor na avaliação inicial, consulta, tratamento por consulta e interação de consulta por valor na avaliação inicial. Uma alteração desde a Avaliação Inicial de 0 foi imputada na primeira consulta pós-avaliação inicial, para qualquer participante sem um valor pós-avaliação inicial.
No Estudo 2, a melhora da proptose medida pela alteração média desde a Avaliação Inicial foi observada já em 6 semanas e continuou a melhorar até a semana 24, conforme mostrado na Figura 1. Resultados semelhantes foram observados no Estudo 1.
Figura 1. Alteração desde a avaliação inicial na proptose ao longo de 24 semanas no Estudo 2
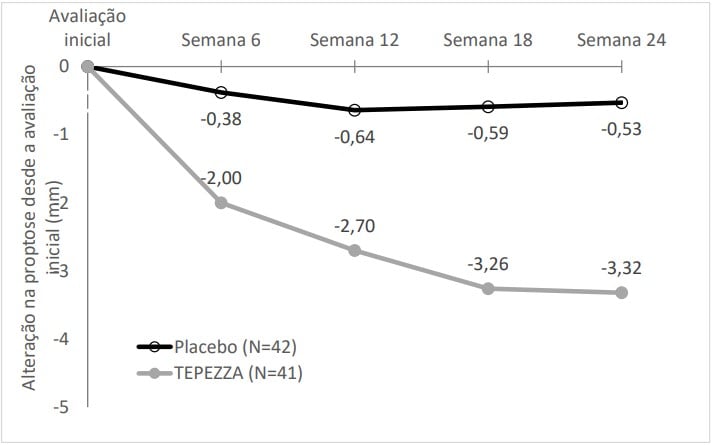
P<0,01 em cada momento.
Teprotumumabe também levou a uma melhora no olho “ipsolateral” menos gravemente afetado.
A diplopia (visão dupla) foi avaliada em um subgrupo de pacientes que apresentavam diplopia na avaliação inicial nos Estudos 1 e 2. Os resultados são mostrados na Tabela 2.
Tabela 2. Diplopia em pacientes com Doença Ocular da Tireoide nos Estudos 1 e 2
| Parâmetro | Teprotumumabe (n=66) | Placebo (n=59) |
| Diplopia Taxa de respondedora na semana 24, % (n) | 53% (35) | 25% (15) |
P<0,01.
a A diplopia foi avaliada em uma escala de 4 pontos em que as pontuações variaram de 0 para nenhuma diplopia a 3 para diplopia constante. Um respondedor de diplopia foi definido como um paciente com diplopia na avaliação inicial >0 e uma pontuação de 0 na semana 24.
Após a interrupção do tratamento no Estudo 1, 53% dos pacientes (16 de 30 pacientes) que eram respondedores para proptose na semana 24 mantiveram a resposta à proptose 51 semanas após a última infusão de teprotumumabe. 67% dos pacientes (12 de 18 pacientes) que eram respondedores para diplopia na semana 24 mantiveram a resposta à diplopia 51 semanas após a última infusão de teprotumumabe.
Subgrupos
O exame dos subgrupos de idade e gênero não identificou diferenças na resposta a teprotumumabe entre esses subgrupos. A redução na proptose foi semelhante entre fumantes e não fumantes em ambos os estudos.
Características Farmacológicas
Propriedades farmacodinâmicas
Grupo farmacoterapêutico: imunossupressores, imunossupressores seletivos, código ATC L04AA53.
Teprotumumabe é um anticorpo monoclonal de IgG1 totalmente humano, inibidor do receptor do fator de crescimento semelhante à insulina-1 (IGF-1R), indicado para o tratamento da Doença Ocular da Tireoide ativa.
Não foram realizados estudos formais de farmacodinâmica com teprotumumabe.
Mecanismo de ação
O mecanismo de ação de teprotumumabe em pacientes com Doença Ocular da Tireoide ativa não foi totalmente caracterizado. Teprotumumabe se liga a IGF-1R e bloqueia sua ativação e sinalização.
Propriedades farmacocinéticas
A farmacocinética (PK) de teprotumumabe foi descrita por um modelo de PK populacional de dois compartimentos, baseado em dados de 40 pacientes com Doença Ocular da Tireoide que receberam uma infusão intravenosa inicial de 10 mg/kg, seguida por infusões de 20 mg/kg de teprotumumabe a cada 3 semanas em um estudo clínico. Após esse esquema, as estimativas médias (± desvio padrão) da área sob a curva (AUC) de concentração em estado de equilíbrio, concentrações de pico (Cmax) e vale (Cvale) de teprotumumabe foram 138 (± 34) mg•hr/mL, 632 (± 139) mg/mL e 176 (± 56) mg/mL, respectivamente.
Distribuição
Após o esquema de dosagem recomendado de teprotumumabe, a PK populacional média estimada (± desvio padrão) para o volume de distribuição central e periférico de teprotumumabe foi 3,26 L (± 0,87 L) e 4,32 L (± 0,67 L), respectivamente. A depuração intercompartimental média (± desvio padrão) estimada foi 0,74 L/dia (± 0,16 L/dia).
Eliminação
Após o esquema de dosagem recomendado de teprotumumabe, a PK populacional média estimada (± desvio padrão) para a depuração de teprotumumabe foi 0,27 L/dia (± 0,08 L/dia) e para a meia-vida de eliminação foi 20 dias (± 5 dias).
Metabolismo
O metabolismo de teprotumumabe não foi totalmente caracterizado. No entanto, é previsto que teprotumumabe sofra metabolismo por proteólise.
Populações especiais
Nenhuma diferença significativa em termos clínicos na farmacocinética de teprotumumabe foi observada após a administração de teprotumumabe com base na idade do paciente (18-80 anos), gênero, raça/etnia (103 brancos, 10 negros e 3 asiáticos), peso (46-169 kg), insuficiência renal leve a moderada (depuração de creatinina 30 a 89 mL/min estimada pela Equação de Cockcroft-Gault), níveis de bilirrubina (2,7-24,3 mmol/L), níveis de aspartato aminotransferase (AST) (11-221 U/L) ou níveis de alanina aminotransferase (ALT) (7-174 U/L). O efeito da insuficiência hepática na farmacocinética de teprotumumabe é desconhecido.
Uso em idosos
Entre os 171 pacientes nos dois estudos randomizados, 15% tinham 65 anos ou mais; o número de pacientes com 65 anos ou mais foi semelhante entre os grupos de tratamento. Não foram observadas diferenças globais na eficácia ou segurança entre pacientes com 65 anos ou mais e pacientes mais jovens (menos de 65 anos de idade).
Uso pediátrico
A segurança e a efetividade não foram estabelecidas em pacientes pediátricos.
Carcinogênese, mutagênese, comprometimento da fertilidade
Carcinogênese
O potencial carcinogênico de teprotumumabe não foi avaliado em estudos a longo prazo com animais.
Mutagênese
O potencial genotóxico de teprotumumabe não foi avaliado.
Comprometimento da fertilidade
Não foram realizados estudos de fertilidade com teprotumumabe.

 Revisado por Isabelle Baião de Mello Neto (CRF-MG 24309)
Revisado por Isabelle Baião de Mello Neto (CRF-MG 24309)