Qual a ação da substância do Tasigna?
Resultados de Eficácia
LMC Ph+-FC recém-diagnosticada
Um estudo de fase III randomizado, aberto e multicêntrico foi conduzido para determinar a eficácia de Nilotinibe versus imatinibe em pacientes adultos com LMC Ph+-FC confirmada por citogenética e recém-diagnosticados. Os pacientes incluídos no estudo estavam dentro dos 6 primeiros meses após o diagnóstico e não foram previamente tratados para LMC-FC, exceto por hidroxiureia e/ou anagrelida. Adicionalmente, os pacientes foram estratificados de acordo com o risco de Sokal no momento do diagnóstico.
A eficácia foi baseada em um total de 846 pacientes (283 pacientes no grupo de imatinibe 400 mg uma vez ao dia, 282 pacientes no grupo de Nilotinibe 300 mg duas vezes ao dia, 281 pacientes no grupo de Nilotinibe 400 mg duas vezes ao dia).
As características basais foram bem balanceadas entre os três grupos. A idade mediana foi de 46 anos no grupo de imatinibe e de 47 anos nos dois grupos de Nilotinibe, sendo que 12,4%, 12,8% e 10,0% tinham ≥ 65 anos de idade nos grupos de tratamento de imatinibe, Nilotinibe 300 mg duas vezes ao dia e Nilotinibe 400 mg duas vezes ao dia, respectivamente. Houve um pouco mais de pacientes homens do que mulheres em todos os grupos (55,8%, 56,0% e 62,3% nos grupos de imatinibe, Nilotinibe 300 mg duas vezes ao dia e Nilotinibe 400 mg duas vezes ao dia, respectivamente). Mais do que 60% de todos os pacientes eram caucasianos, e 25% eram asiáticos.
O período de análise primária dos dados foi quando todos os 846 pacientes completaram 12 meses de tratamento (ou descontinuaram precocemente). A análise subsequente reflete quando os pacientes completaram 24, 36, 48 e 60 meses de tratamento (ou descontinuaram precocemente). O tempo mediano em tratamento foi de aproximadamente 60 meses em todos os três grupos de tratamento. A dose mediana atual foi de 400 mg/dia no grupo de imatinibe, 593 mg/dia no grupo de Nilotinibe 300 mg duas vezes ao dia e 773 mg/dia no grupo de Nilotinibe 400 mg duas vezes ao dia. Este estudo está em andamento.
Resposta molecular maior (RMM)
A variável primária de eficácia foi RMM aos 12 meses após o início da medicação do estudo. RMM foi definida como ≤ 0,1% BCR-ABL/ABL % pela escala internacional medida por RQ-PCR, que corresponde a uma redução ≥ 3 log de transcritos BCR-ABL a partir do nível basal padronizado.
O desfecho primário de eficácia, a taxa de RMM aos 12 meses, foi estatisticamente e significantemente superior no grupo de Nilotinibe 300 mg duas vezes ao dia comparado ao grupo de imatinibe 400 mg uma vez ao dia (44,3% vs22,3%, p < 0,0001). A taxa de RMM aos 12 meses, também foi estatisticamente e significantemente superior no grupo de Nilotinibe 400 mg duas vezes ao dia comparado ao imatinibe 400 mg uma vez ao dia (42,7% vs 22,3%, p < 0,0001), Tabela 1.
Na dose recomendada de Nilotinibe 300 mg duas vezes ao dia, as taxas de RMM aos 3, 6, 9 e 12 meses foram 8,9%, 33,0%, 43,3% e 44,3%. No grupo de Nilotinibe 400 mg duas vezes ao dia, as taxas de RMM aos3, 6, 9 e 12 meses foram 5,0%, 29,5%, 38,1% e 42,7%. No grupo de imatinibe 400 mg uma vez ao dia, as taxas de RMM aos 3, 6, 9 e 12 meses foram 0,7%, 12,0%, 18,0% e 22,3%.
As taxas de RMM aos 12, 24, 36, 48 e 60 meses estão demonstradas na Tabela 1.
Tabela 1 – Taxa de RMM
| - | Nilotinibe 300 mg 2 x ao dia n = 282 n (%) | Nilotinibe 400 mg 2 x ao dia n = 281 n (%) | Imatinibe 400 mg 1 x ao dia n = 283 n (%) |
RMM aos 12 meses | 125 (44,3)1 | 120 (42,7)1 | 63 (22,3) |
IC de 95% para resposta | [38,4,50,3] | [36,8,48,7] | [17,6,27,6] |
RMM aos 24 meses | 174 (61,7)1 | 166 (59,1)1 | 106 (37,5) |
IC de 95% para resposta | [55,8,67,4] | [53,1,64,9] | [31,8,43,4] |
RMM aos 36 meses2 | 165 (58.5)1 | 161 (57.3)1 | 109 (38.5) |
IC de 95% para resposta | [52,5,64,3] | [51,3,63,2] | [32,8,44,5] |
RMM aos 48 meses3 | 169 (59,9)1 | 155 (55,2) | 124 (43,8) |
IC de 95% para resposta | [54,0,65,7] | [49,1,61,1] | [38,0,49,8] |
RMM aos 60 meses4 | 177 (62,8) | 172 (61,2) | 139 (49,1) |
IC de 95% para resposta | [56,8,68,4] | [55,2,66,9] | [43,2,55,1] |
1 CMH teste p-valor de taxa de resposta (vs. imatinibe 400 mg) < 0,0001.
2 Apenas os pacientes que estavam em RMM, num ponto específico foram incluídos como respondedores para esse ponto. Um total de 199 (35,2%) de todos os pacientes não foram avaliáveis para RMM em 36 meses (87 no grupo de 300 mg de Nilotinibe duas vezes ao dia e 112 no grupo do imatinibe), devido à falta de avaliações de PCR/não avaliáveis (n = 17), transcrições atípicas no início do estudo (n = 7), ou a suspensão antes do ponto de 36 meses (n = 175).
3 Apenas os pacientes que estavam em RMM, num ponto específico foram incluídos como respondedores para esse ponto. Um total de 305 (36,1%) de todos os pacientes não foram avaliáveis para RMM em 48 meses (98 no grupo de 300 mg de Nilotinibe duas vezes ao dia, e 88 no grupo de 400 mg de Nilotinibe duas vezes por dia e 119 no grupo de imatinibe), devido à falta/não avaliáveis PCR (n = 18), transcrições atípicas no início do estudo (n = 8), ou a suspensão antes do ponto de 48 meses (n = 279).
4 Apenas pacientes que estavam em RMM, num ponto específico foram incluídos como respondedores para este ponto. Um total de 322 (38,1%) de todos os pacientes não foram avaliáveis para RMM em 60 meses (99 no grupo de 300 mg de Nilotinibe duas vezes ao dia, 93 no grupo de 400 mg de Nilotinibe duas vezes por dia e 130 no grupo de imatinibe) devido à falta/não avaliáveis de PCR (n = 9), das transcrições atípicas na linha de base (n = 8) ou suspensão antes do ponto de 60 meses (n = 305).
Taxas de RMM nos diferentes pontos (incluindo pacientes que atingiram RMM no ponto ou antes daqueles pontos como respondedores) estão apresentados na incidência cumulativa de RMM (Figura 1).
Figura 1 – Incidência cumulativa de RMM
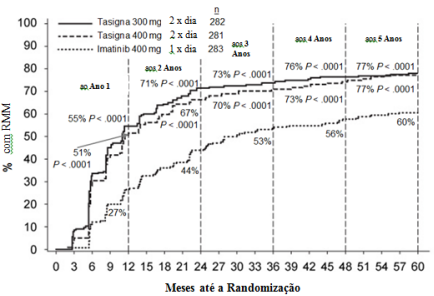
Para todos os grupos de risco Sokal, as taxas de RMM em todos os intervalos de tempo permaneceram consideravelmente maiores nos dois grupos de Nilotinibe do que no grupo de imatinibe.
Em uma análise retrospectiva, 91% (234/258) dos pacientes que receberam Nilotinibe 300 mg duas vezes ao dia, atingiram níveis BCR-ABL ≤ 10% em 3 meses de tratamento em comparação com 67% (176/264) dos pacientes tratados com 400 mg de imatinibe uma vez ao dia. Pacientes com níveis de BCR-ABL ≤ 10% em 3 meses de tratamento, demonstraram uma maior sobrevida global em 60 meses, em comparação com aqueles que não alcançaram esse nível de resposta molecular (97% vs 82%, respectivamente [p = 0,0116]).
Com base na análise de Kaplan-Meier do tempo para a primeira RMM, entre todos os pacientes, a probabilidade de alcançar a RMM em diferentes pontos foram maiores em ambos os grupos de Nilotinibe em comparação com o grupo de imatinibe (HR = 2,20 e log-rank estratificado p ˂ 0,0001 entre Nilotinibe 300 mg duas vezes ao dia e imatinibe, HR = 1,88 e log-rank estratificado p ˂ 0,0001 entre Nilotinibe 400 mg duas vezes ao dia e imatinibe).
As proporções de pacientes que tiveram uma resposta molecular de ≤ 0,01% e ≤ 0,0032% na Escala Internacional (EI) em diferentes pontos são apresentadas na Tabela 2 e a proporção de pacientes que tiveram uma resposta molecular de ≤ 0,01% e ≤ 0,0032% na EI por diferentes pontos de tempo, são demonstrados nas Figuras 2 e 3. Resposta moleculares de ≤ 0,01% e ≤ 0,0032% na EI corresponde a ≥ 4 log redução e ≥ 4,5 log redução respectivamente, de transcritos BCRABL a partir de uma base padronizada.
Tabela 2 – Proporção de pacientes que tiveram resposta molecular de ≤ 0,01% (redução de 4 logs) e ≤ 0,0032% (redução de 4,5 logs)
| - | Nilotinibe 300 mg 2x ao dia n = 282 (%) | Nilotinibe 400 mg 2x ao dia n = 281 (%) | Imatinibe 400 mg 1x ao dia n = 283 (%) | |||
| - | ≤ 0,01% | ≤ 0,0032% | ≤ 0,01% | ≤ 0,0032% | ≤ 0,01% | ≤ 0,0032% |
12 meses | 11,7 | 4,3 | 8,5 | 4,6 | 3,9 | 0,4 |
24 meses | 24,5 | 12,4 | 22,1 | 7,8 | 10,2 | 2,8 |
36 meses | 29,4 | 13,8 | 23,8 | 12,1 | 14,1 | 8,1 |
48 meses | 33,0 | 16,3 | 29,9 | 17,1 | 19,8 | 10,2 |
60 meses | 47,9 | 32,3 | 43,4 | 29,5 | 31,1 | 19,8 |
Figura 2 – Incidência cumulativa de resposta molecular de ≤ 0,01% (4 log redução)
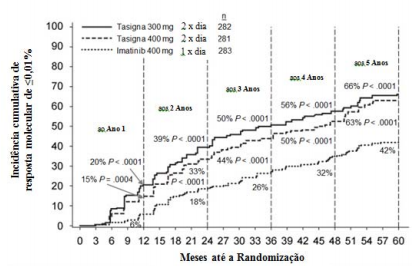
Figura 3 – Incidência cumulativa de resposta molecular de ≤ 0,0032% (4,5 log redução)
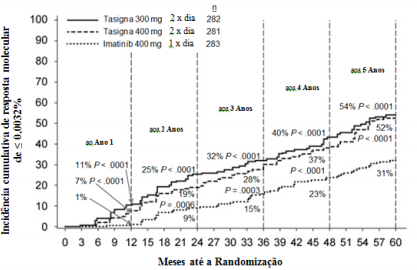
Duração da RMM
Com base nas estimativas de Kaplan-Meier da duração da primeira RMM, as proporções de pacientes que mantiveram a resposta após 60 meses entre os pacientes que atingiram RMM foram de 93,4% (IC de 95%: 89,9% a 96,9%) no grupo Nilotinibe 300 mg duas vezes ao dia, 92,0% (IC de 95%: 88,2% a 95,8%) no grupo Nilotinibe 400 mg duas vezes ao dia e 89,1% (IC de 95%: 84,2% a 94,0%) no grupo imatinibe 400 mg uma vez ao dia.
Resposta citogenética completa (RCC)
A RCC foi definida como 0% de metáfases Ph+ na medula óssea, baseado em um mínimo de 20 metáfases avaliadas. A taxa de RCC em 12 meses (inclui pacientes que atingiram RCC no período de 12 meses ou antes como respondedores) foi estatisticamente superior para ambos os grupos de Nilotinibe 300 mg duas vezes ao dia e 400 mg duas vezes ao dia comparado ao grupo de imatinibe 400 mg uma vez ao dia, Tabela 3.
A taxa de RCC em 24 meses (inclui pacientes que atingiram RCC antes ou em 24 meses como respondedores) foi estatisticamente superior para ambos os grupos de Nilotinibe 300 mg duas vezes ao dia e 400 mg duas vezes ao dia em comparação com imatinibe 400 mg uma vez ao dia.
Após a visita do mês 24, as avaliações citogenéticas não foram necessárias para todos os pacientes e, portanto, nenhuma atualização é fornecida com maior tempo de seguimento sobre as taxas de RCC.
Tabela 3 – Taxa de RCC
| - | Nilotinibe 300 mg 2x ao dia n = 282 n (%) | Nilotinibe 400 mg 2x ao dia n = 281 n (%) | Imatinibe 400 mg 1x ao dia n = 283 n (%) |
12 meses | |||
Resposta citogenética completa | 226 (80,1) | 219 (77,9) | 184 (65,0) |
IC de 95% para resposta | [75,0; 84,6] | [72,6; 82,6] | [59,2; 70,6] |
Valor de p do teste CMH para taxa de resposta (vs. imatinibe 400 mg) | < 0,0001 | 0,0005 | - |
24 meses | |||
Resposta citogenética completa | 245 (86,9%) | 238 (84,7%) | 218 (77,0%) |
IC de 95% para resposta | [82,4, 90,6] | [79,9, 88,7] | [71,7, 81,8] |
Valor de p do teste CMH para taxa de resposta (vs. imatinibe 400 mg) | 0,0018 | 0,0160 | - |
Duração de RCC
Com base nas estimativas de Kaplan-Meier, a proporção de pacientes que mantiveram a resposta após 60 meses entre os pacientes que atingiram RCC foi de 99,1% (IC de 95%: 97,9% a 100%) no grupo de Nilotinibe 300 mg duas vezes ao dia, 98,7% (IC de 95%: 97,1% a 100%) no grupo Nilotinibe 400 mg duas vezes ao dia e 97,0% (IC de 95%: 94,7% a 99,4%) no grupo de imatinibe 400 mg uma vez ao dia.
Progressão para Fase Acelerada (FA)/ Crise Blastica (CB) durante o tratamento
A progressão para FACB no estudo é definida como o tempo desde a data da randomização à primeira progressão da doença documentada para FA/CB ou morte relacionada com a LMC (no tratamento principal, no tratamento de extensão ou em seguimento após descontinuação). A progressão para FA ou CB no estudo foi observada em um total de 37 pacientes: 10 pacientes no grupo Nilotinibe 300 mg duas vezes por dia, 6 pacientes no grupo Nilotinibe 400 mg duas vezes ao dia e 21 pacientes no grupo imatinibe 400 mg uma vez por dia. As taxas estimadas de pacientes sem progressão para FA ou CB aos 60 meses foram 96,3%, 97,8% e 92,1%, respectivamente (HR = 0,4636 e estratificada de log-rank p = 0,0403 entre Nilotinibe 300 mg duas vezes por dia e imatinibe uma vez por dia , HR = 0,2753 e estratificada de log-rank p = 0,0028 entre Nilotinibe 400 mg duas vezes por dia e imatinibe uma vez por dia).
Incluindo a evolução clonal como um critério para a progressão, um total de 25 pacientes evoluíram para FA ou CB em tratamento até a data de corte (3 no grupo de Nilotinibe 300 mg duas vezes ao dia, 5 no grupo do Nilotinibe 400 mg duas vezes ao dia e 17 no grupo do imatinibe 400 mg uma vez ao dia). As taxas estimadas de pacientes sem progressão para FA ou CB incluindo a evolução clonal aos 60 meses foram 98,7%, 97,9% e 93,2% respectivamente (HR = 0,1626 e logrank estratificado p = 0,0009 entre 300 mg de Nilotinibe duas vezes ao dia e imatinibe, HR = 0,2848 e log-rank estratificado p = 0,0085 entre 400 mg de Nilotinibe duas vezes ao dia e imatinibe).
Sobrevida livre de progressão (SLP)
Os resultados da análise de SLP no tratamento principal e em estudo são apresentados na Tabela 4.
Tabela 4 – Sobrevida livre de progressão (SLP)
| - | Nilotinibe 300 mg 2x ao dia (n = 282) | Nilotinibe 400 mg 2x ao dia (n = 281) | Imatinibe 400 mg 1x ao dia (n = 283) |
SLP estimada durante 5 anos no tratamento principal, % | 96,5 | 98,3 | 94,7 |
Progressões e mortes, n | 8 | 4 | 13 |
Razão de risco (IC de 95%) vs. imatinibe | 0,5684 (0,2354- 1,3729) | 0,3011 (0,0981- 0,9241) | - |
Valor de p vs. imatinibe | 0,2032 | 0,0260 | - |
SLP estimada durante 5 anos no estudo, % | 92,2 | 95,8 | 91,0 |
Progressões e mortes, n | 22 | 11 | 24 |
Razão de risco (IC de 95%) vs. imatinibe | 0,8883 (0,4980- 1,5843) | 0,4399 (0,2155- 0,8981) | - |
Valor de p vs. imatinibe | 0,6879 | 0,0204 | - |
Sobrevida livre de eventos (SLE)
Os resultados da análise de SLE no tratamento principal estão demonstrados na Tabela 5.
Tabela 5 – Sobrevida livre de eventos (SLE)
| - | Nilotinibe 300 mg 2x ao dia (n = 282) | Nilotinibe 400 mg 2x ao dia (n = 281) | Imatinibe 400 mg 1x ao dia (n = 283) |
SLE estimada através da análise KaplanMeier durante 5 anos no tratamento principal, % | 95,0 | 96,9 | 92,6 |
Eventos de SLE, na | 12 | 7 | 18 |
Razão de risco (IC de 95%) vs. imatinibe | 0,6145 (0,2957-1,2767) | 0,3656 (0,1525-0,8769) | - |
Valor de p vs. imatinibe | 0,1874 | 0,0188 | - |
ª Eventos de SLE incluíram morte de qualquer natureza, progressão para FA/CB, e perda de resposta citogenética parcial, RCC, ou resposta hematológica completa.
Sobrevida global (SG)
Os resultados da análise de SG e mortes relacionadas à LMC são apresentados na Tabela 6.
Tabela 6 – Sobrevida global e mortes relacionadas à LMC
| - | Nilotinibe 300 mg 2x ao dia (n = 282) | Nilotinibe 400 mg 2x ao dia (n = 281) | Imatinibe 400 mg 1x ao dia (n = 283) |
Total de mortes, na | 18 | 10 | 22 |
SG estimada através da análise Kaplan-Meier durante 5 anos, % | 93,7 | 96,2 | 91,7 |
Razão de risco vs. imatinibe (IC de 95%) | 0,8026 (0,4305-1,4964) | 0,4395 (0,2081-0,9281) | - |
Valor de p vs. imatinibe | 0,4881 | 0,0266 | - |
Mortes em pacientes com LMC avançada, nb | 6 | 4 | 16 |
SG estimada através da análise Kaplan-Meier durante 5 anos, % | 97,7 | 98,5 | 93,8 |
Razão de risco vs. imatinibe (IC de 95%) | 0,3673 (0,1437-0,9387) | 0,2411 (0,0806-0,7214) | - |
Valor de p vs. imatinibe | 0,0292 | 0,0057 | - |
a Eventos de SG incluíram morte de qualquer natureza a qualquer momento (no tratamento principal, no tratamento de extensão ou durante o acompanhamento após a descontinuação do tratamento).
b Pacientes para os quais a causa principal de morte foi “indicação do estudo”. Adicionalmente, pacientes com causa de morte “desconhecida” ou não reportada, porém que tenha ocorrido subsequentemente a uma progressão FA/CB documentada.
LMC Ph+ após falha ou intolerância
Um estudo aberto, multicêntrico, de fase II foi conduzido para determinar a eficácia de Nilotinibe (400 mg duas vezes ao dia) em pacientes com LMC após falha ou intolerância ao imatinibe, com braços separados de tratamento para as fases crônica (FC) e acelerada (FA) da doença. A eficácia foi baseada em 321 pacientes envolvidos em FC e em 137 pacientes envolvidos em FA. A duração mediana do tratamento foi de 561 dias e 264 dias, respectivamente (vide Tabela 7). Nilotinibe foi administrado continuamente (duas vezes ao dia, 2 horas após a refeição e sem alimentação adicional após pelo menos uma hora) a menos que houvesse uma evidência de resposta inadequada ou de progressão da doença. O escalonamento da dose para 600 mg duas vezes ao dia foi permitido.
Tabela 7 – Duração da exposição ao Nilotinibe
| - | Fase crônica (FC) n = 321 | Fase acelerada (FA) n = 137 |
Duração média da terapia em dias | 561 (196 - 852) | 264 |
Os critérios considerados na resistência ou falha ao imatinibe incluíram falha para obter resposta hematológica completa (após 3 meses), resposta citogenética (após 6 meses) ou resposta citogenética maior (após 12 meses) ou progressão da doença após resposta citogenética ou hematológica prévia. Os critérios considerados na intolerância ao imatinibe incluíram pacientes que descontinuaram imatinibe devido à toxicidade e por não apresentarem resposta citogenética maior na ocasião em que ingressaram no estudo.
Em geral, 73% dos pacientes eram resistentes e 27% eram intolerantes ao imatinibe. A maioria dos pacientes tinha um longo histórico de LMC, que incluía extensos tratamentos anteriores com outros agentes antineoplásicos, tais como, imatinibe, hidroxiureia, interferona e alguns destes pacientes também apresentavam transplante de medula óssea prévio mal sucedido. A média da dose anterior mais alta de imatinibe foi de 600 mg/dia para pacientes em FC e em FA, e a dose anterior mais alta de imatinibe foi ≥ 600 mg/dia em 74% de todos pacientes, sendo 40% dos pacientes com doses prévias de imatinibe ≥ 800 mg/dia.
Tabela 8 – Histórico das características da LMC
| - | Fase crônica (FC) (n = 321) | Fase acelerada (FA) (n = 137)* |
Tempo médio desde o diagnóstico em meses (intervalo) | 58 (5 - 275) | 71 |
Terapia com imatinibe | ||
Falha | 226 (70%) 95 (30%) | 109 (80%) |
Tempo médio de tratamento com imatinibe em dias | 976 (519 - 1.488) | 857 |
Terapia anterior com hidroxiureia | 83% | 91% |
Terapia anterior com interferona | 58% | 50% |
Transplante de medula óssea prévio | 7% | 8% |
*Faltam informações de um paciente referente à tolerância/ resistência ao imatinibe.
O desfecho primário nos pacientes em FC foi a resposta citogenética maior (RCM), definida como eliminação (RCC, resposta citogenética completa) ou redução significante para < 35% das metáfases Ph+ (resposta citogenética parcial) das células hematopoiéticas Ph+. A resposta hematológica completa (RHC) em pacientes na FC foi avaliada como um desfecho secundário. O desfecho primário nos pacientes em FA foi a resposta hematológica (RH) global confirmada, definida também como uma resposta hematológica completa, nenhuma evidência de leucemia ou retorno à fase crônica.
Fase crônica
A taxa de RCM nos 321 pacientes em FC foi 59%. A maioria dos respondedores atingiu rapidamente a RCM, dentro de 3 meses (média de 2,8 meses) a partir do início do tratamento com Nilotinibe, e estas respostas foram mantidas. A taxa de RCC foi de 44%. O tempo médio para atingir RCC foi de 3 meses (média de 3,3 meses). Dos pacientes que atingiram RCM, 77% (IC 95%: 71%-84%) manteve a resposta aos 24 meses. A duração média da RCM não foi atingida. Dos pacientes que atingiram RCC, 84% (IC 95%: 77%-91%) mantiveram a resposta aos 24 meses. A duração média da RCC não foi atingida. Pacientes com RHC ao início atingiram RCM mais rápido (1,4 vs 2,8 meses).
Dos pacientes em FC sem RHC ao início, 76% atingiram RHC, e o tempo médio para a RHC foi de 1 mês, com a duração média ainda não atingida.
A taxa de sobrevida global estimada aos 24 meses para pacientes com LMC – FC foi de 87%.
Fase acelerada
A taxa global de RH confirmada em 137 pacientes em FA foi de 55%. A maioria dos respondedores atingiu precocemente a RH no tratamento com Nilotinibe (média de 1 mês) e isto foi duradouro (duração média de RH confirmada foi de 21,5 meses). Dos pacientes que atingiram RH, 49% (IC 95%: 35%-62%) mantiveram resposta aos 24 meses. A taxa de RCM foi de 32% com tempo médio para resposta de 2,8 meses. Dos pacientes que atingiram RCM, 66% (IC 95%: 50%-82%) mantiveram resposta aos 24 meses. A duração média da RCM não foi atingida. As taxas de resposta para os dois braços de tratamentos estão relatadas na Tabela 9.
A taxa de sobrevida total estimada aos 24 meses para pacientes com LMC – FA foi de 70%.
Tabela 9 – Taxa de resposta em LMC
(Melhor taxa de resposta) | Fase crônica | Fase acelerada | ||||
Intolerância (n = 95) | Falha (n = 226) | Total (n = 321) | Intolerância (n = 27) | Falha (n = 109) | Total* (n = 137) | |
Resposta hematológica (%) | - | - | - | 56 (35-75) | 55 (45-65) | 55 (47-64) |
Global (IC 95%) | - | - | - | - | - | - |
Completa | 90 (79-97) | 72 (64-79) | 761 (70-82) | 37 | 30 | 31 |
SEL | - | - | - | 15 | 11 | 12 |
Retorno à Fase crônica | - | - | - | 4 | 14 | 12 |
Resposta citogenética (%) | - | - | - | - | - | - |
Maior (IC 95%) | 66 (56-76) | 56 (49-63) | 59 (54-65) | 41 (22-61) | 30 (22-40) | 32 (24-41) |
Completa | 51 | 41 | 44 | 30 | 19 | 21 |
Parcial | 16 | 15 | 15 | 11 | 11 | 11 |
SEL = sem evidência de leucemia/resposta medular.
1 – 114 pacientes em fase crônica apresentavam RHC ao início do estudo e não foram avaliados para resposta hematológica completa.
* Faltam informações de um paciente referente à tolerância/resistência ao imatinibe.
Os braços separados de tratamento também foram incluídos no estudo de fase II para avaliar Nilotinibe em um grupo de pacientes em FC e FA, que foram extensivamente pré-tratados com múltiplas terapias incluindo agentes inibidores da tirosinoquinase em adição ao imatinibe. Destes pacientes, 30/36 (83%) eram resistentes ao tratamento. Em 22 pacientes em FC avaliados para eficácia, Nilotinibe induziu uma taxa de RCM em 32% e uma taxa de RHC de 50%. Em 11 pacientes em FA avaliados para eficácia, o tratamento induziu uma taxa de RH global de 36%.
Após falha do imatinibe, 24 mutações diferentes do BCR-ABL foram observadas em 42% dos pacientes com LMC em fase crônica e 54% dos pacientes com LMC em fase acelerada que foram avaliados para mutações. Nilotinibe demonstrou eficácia em pacientes com presença de uma variedade de mutações do BCR-ABL associadas com resistência ao imatinibe, exceto T315I.
Adicionalmente, com o objetivo de confirmar o perfil de segurança do Nilotinibe em uma população maior de pacientes, o estudo 2109, um estudo fase 3, aberto, multicêntrico, internacional, em pacientes adultos com LMC em fase crônica, fase acelerada e crise blástica, resistentes ou intolerantes ao imatinibe foi conduzido. Em comparação com o estudo fase 2 anteriormente descrito, o número total de pacientes do estudo 2109 com LMC em fase crônica e em fase acelerada foi de 1.219 e 157 pacientes respectivamente. Na população em FC, 566 foram avaliados para resposta hematológica e 532 foram avaliados para resposta citogenética. No grupo em FA, 90 pacientes foram avaliados para resposta hematológica e 84 pacientes para resposta citogenética, respectivamente.
Nos pacientes com LMC em FC, foi observada uma taxa de resposta hematológica de 62%, sendo 41% resposta hematológica completa. Em relação à resposta citogenética, obteve-se uma taxa de resposta citogenética maior de 42%, sendo 26% resposta citogenética completa e 15% parcial. A duração mediana de exposição ao Nilotinibe nos pacientes em FC foi de 184 dias.
Nos pacientes com LMC em FA, a taxa de resposta hematológica foi de 44%, sendo 22% em resposta hematológica completa, e uma taxa de resposta citogenética maior de 12%, sendo 6% às custas de resposta citogenética completa e 6% parcial. Retornaram à fase crônica 10% dos pacientes e 12% não tinham evidência de leucemia ao exame da medula óssea. A duração mediana de exposição ao Nilotinibe nos pacientes em FA foi de 137 dias.
Referências Bibliográficas
1. Study 2101E2 (Study 2101 CP CSR). Study 2101 (Phase II component, imatinib-resistant/intolerant CML-chronic phase): A Phase IA/II, multicenter, doseescalation study of oral AMN107 on a continuous daily dosing schedule in adult patients with Gleevec® (imatinib)- resistant/intolerant CML in chronic or accelerated phase or blast crisis, relapsed/refractory Ph+ALL, and other hematologic malignancies. Module 5, Vol. 57, Section/Page 5.3.5.2/17782.
2. Imatinib-resistant/intolerant Chronic Myelogenous Leukemia (CML) in Chronic Phase (CP) or Accelerated Phase (AP). 2.7.3 Summary of Clinical Efficacy in CML-CP or CML-AP 120-Day Update. Novartis Pharma AG. Basel, Switzerland. 16 Jan 07.
3. Study 2101E1 (Study 2101 AP CSR). Study 2101 (Phase II component, imatinib-resistant/intolerant CML-accelerated phase): A Phase IA/II, multicenter, dose-escalation study of oral AMN107 on a continuous daily dosing schedule in adult patients with Gleevec® (imatinib)-resistant/intolerant CML in chronic or accelerated phase or blast crisis, relapsed/refractory Ph+ALL, and other hematologic malignancies. Module 5, Vol. 97, Section/Page 5.3.5.2/35666.
4. Summary of Clinical Efficacy. Module 2, Vol. 3, Section/Page 2.7.3/1.
5. Clinical Overview (2010) – Nilotinib for treatment of CML-CP or CML-AP, Novartis Pharma AG, Basel, Switzerland, February 22, 2010 (provides 24 month update to efficacy and safety sections of Novartis Core Data Sheet).
6. Study 2101E2 (Study 2101 CP CSR with 24 month update). Study 2101 (Phase II component, imatinibresistant/intolerant CML-chronic phase): A Phase IA/II, multicenter, dose-escalation study of oral AMN107 on a continuous daily dosing schedule in adult patients with Gleevec® (imatinib)-resistant/intolerant CML in chronic or accelerated phase or blast crisis, relapsed/refractory Ph+ALL, and other hematologic malignancies. Clinical Study Report CAMN107A2101E2. 16 Oct 09.
7. Study 2101E1 (Study 2101 AP CSR with 24 month update). Study 2101 (Phase II component, imatinibresistant/intolerant CML-accelerated phase): A Phase IA/II, multicenter, dose-escalation study of oral AMN107 on a continuous daily dosing schedule in adult patients with Gleevec® (imatinib)-resistant/intolerant CML in chronic or accelerated phase or blast crisis, relapsed/refractory Ph+ALL, and other hematologic malignancies. Clinical Study Report CAMN107A2101E1. 04 Nov 09.
Características Farmacológicas
Grupo farmacoterapêutico: agentes antineoplásicos – inibidor da proteína tirosinoquinase.
Código ATC: L01XE08.
Propriedades farmacodinâmicas
Nilotinibe é um potente e seletivo inibidor da atividade–tirosinoquinase-ABL da oncoproteína BCR-ABL em linhagens celulares e principalmente em células leucêmicas cromossomo Philadelphia positivo. O medicamento se liga fortemente ao sítio de ligação do ATP de tal forma que se torna um potente inibidor do tipo selvagem da BCR-ABL e mantém atividade contra 32 das 33 formas mutantes da BCR-ABL resistentes ao imatinibe. Como consequência de sua atividade bioquímica, o Nilotinibe inibe seletivamente a proliferação e induz a apoptose em linhagens celulares dependentes de BCR-ABL e, principalmente, em células leucêmicas cromossomo Philadelphia positivo de pacientes com LMC. Em modelos murinos de LMC, em monoterapia com administração oral, Nilotinibe reduz a carga tumoral e prolonga a sobrevida.
Nilotinibe tem pouco ou nenhum efeito sobre a maioria das outras proteínas-quinase avaliadas, incluindo SRC, com exceção dos seguintes receptores de quinase: PDGF, KIT, CSF-1R, DDR e efrina, os quais são inibidos nas concentrações médias atingidas após administração oral nas doses terapêuticas recomendadas para o tratamento da LMC (vide Tabela 10).
Tabela 10 – Perfil de quinases do Nilotinibe (Fosforilação IC50 nM)
BCR-ABL | PDGFR | KIT |
20 | 69 | 210 |
Propriedades farmacocinéticas
Absorção
Os picos de concentração de Nilotinibe são alcançados 3 horas após a administração oral. A absorção de Nilotinibe após administração oral foi aproximadamente de 30%. A biodisponibilidade absoluta de Nilotinibe não foi determinada. Em comparação com uma solução oral (pH de 1,2 a 1,3), a biodisponibilidade relativa das cápsulas de Nilotinibe é aproximadamente 50%. Em voluntários sadios, a Cmáx e a área sob a curva (AUC) da concentração x tempo do Nilotinibe aumentam em 112% e 82%, respectivamente, quando Nilotinibe é administrado com alimento comparado com jejum. A administração de Nilotinibe 30 minutos ou 2 horas após a refeição aumenta a biodisponibilidade de Nilotinibe para 29% ou 15%, respectivamente. A absorção de Nilotinibe (biodisponibilidade relativa) pode ser reduzida em aproximadamente 48% e 22% em pacientes com gastrectomia total e parcial, respectivamente.
Distribuição
A razão sangue/plasma do Nilotinibe é 0,68. A ligação às proteínas plasmáticas é de aproximadamente 98% com base em estudos in vitro.
Biotransformação/metabolismo
As principais vias metabólicas identificadas em indivíduos sadios são a oxidação e a hidroxilação. O principal componente sérico circulante foi o Nilotinibe, principalmente metabolizado pelo CYP3A4. Nenhum dos metabólitos contribuiu significantemente para a atividade farmacológica do Nilotinibe.
Eliminação
Após uma dose única de Nilotinibe radiomarcado em indivíduos sadios, mais de 90% da dose foi eliminada dentro de 7 dias, principalmente nas fezes. A droga-mãe respondeu por 69% da dose.
A aparente meia-vida de eliminação estimada a partir da farmacocinética de doses múltiplas, em doses diárias, foi de aproximadamente 17 horas. A variabilidade farmacocinética interpaciente do Nilotinibe foi considerada de moderada à alta (CV%: 33% a 43%).
Linearidade/não linearidade
A exposição de Nilotinibe no estado de equilíbrio foi dose-dependente, com aumentos menores do que o proporcional à dose na exposição sistêmica com doses maiores de 400 mg, administradas uma vez ao dia. A exposição sistêmica diária de 400 mg de Nilotinibe, duas vezes ao dia, no estado de equilíbrio, foi 35% maior do que com a administração de 800 mg uma vez ao dia. A exposição sistêmica (AUC) de Nilotinibe no estado de equilíbrio na dose de 400 mg duas vezes ao dia foiaproximadamente 13,4% maior do que com 300 mg duas vezes ao dia. As concentrações médias do pico de Nilotinibe durante 12 meses foram aproximadamente 15,7% e 14,8% maiores com a dose de 400 mg duas vezes ao dia, quando comparadas à dose de 300 mg duas vezes ao dia.
Não houve aumento relevante na exposição ao Nilotinibe quando a dose foi aumentada de 400 mg duas vezes ao dia para 600 mg duas vezes ao dia.
As condições de estado de equilíbrio foram essencialmente alcançadas até o oitavo dia. Um aumento na exposição sistêmica do Nilotinibe, entre a primeira dose e o estado de equilíbrio, foi de aproximadamente 2 vezes para uma dose diária de 400 mg uma vez ao dia e de 3,8 vezes para uma dose diária de 400 mg duas vezes ao dia.
Estudos de biodisponibilidade/bioequivalência
Doses únicas de 400 mg de Nilotinibe, administradas usando 2 cápsulas de 200 mg em que o conteúdo de cada cápsula foi disperso em uma colher de chá de suco de maçã, mostraram ser bioequivalentes em relação a administração única de 2 cápsulas intactas de 200 mg.
Dados de segurança pré-clínica
O Nilotinibe foi avaliado quanto à segurança farmacológica, a toxicidade de dose repetida, a genotoxicidade, em estudos de toxicidade reprodutiva, e fototoxicidade e de carcinogenicidade (ratos e camundongos).
Farmacologia de segurança e toxicidade de dose repetida
O Nilotinibe não teve efeitos no SNC e nas funções respiratórias. Estudos de segurança cardíaca in vitro demonstraram um sinal pré-clínico de prolongamento do intervalo QT. Nenhum efeito foi observado em ECG de cães ou macacos tratados até 39 semanas ou em estudos telemétricos especiais em cães.
Estudos de toxicidade de dose repetida em cães, com duração de até 4 semanas, e em macacos Cynomolgus, com duração de até 9 meses, revelaram que o fígado é o principal órgão afetado pela toxicidade do Nilotinibe. As alterações incluíram o aumento de atividade da alanina aminotransferase e da fosfatase alcalina, e achados histopatológicos (principalmente hiperplasia/hipertrofia das células sinusoidais ou nas células de Kupffer, hiperplasia do canal da bile e fibrose periportal). Em geral, as alterações clínicas e bioquímicas foram totalmente reversíveis após um período de recuperação de quatro semanas, as alterações histológicas apresentaram apenas reversibilidade parcial. Exposições às menores doses que mostraram efeitos hepáticos foram menores que a exposição em humanos na dose de 800 mg/dia. Foram observadas apenas alterações hepáticas pouco importantes em camundongos ou ratos tratados por até 26 semanas. Em ratos, cães e macacos foram observados aumentos geralmente reversíveis nos níveis de colesterol.
Carcinogenicidade e mutagenicidade
Estudos de genotoxicidade em sistemas bacterianos in vitro e em sistemas de mamíferos in vitro e in vivo com e sem ativação metabólica, não revelaram nenhuma evidência de um potencial mutagênico para o Nilotinibe.
No estudo de 2 anos de carcinogenicidade, em ratos não houve nenhuma evidência de carcinogenicidade sobre a administração de Nilotinibe a 5, 15 e 40 mg/kg/dia. Exposições (em termos de AUC) na dose mais elevada estavam representando aproximadamente duas a três vezes a exposição diária humana (baseada na AUC) ao Nilotinibe no estado de equilíbrio na dose de 800 mg/dia. O maior órgão afetado por lesões não neoplásicas foi o útero (dilatação, ectasia vascular, hiperplasia de células endoteliais, inflamação e/ou hiperplasia epitelial).
No estudo de 26 semanas de carcinogenicidade em ratos (Tg.rasH2) no qual foram administrados 30, 100 e 300 mg/Kg/dia, papilomas/carcinomas cutâneos foram detectados a 300 mg/Kg, representando aproximadamente 30 a 40 vezes (baseado na AUC) a exposição humana na dose máxima aprovada de 800 mg/dia (administrada como 400 mg duas vezes/dia). O nível do efeito não observado para as lesões neoplásicas de pele foi de 100 mg/Kg/dia, representando aproximadamente de 10 a 20 vezes a exposição humana na dose máxima aprovada de 800 mg/dia (administrada em 400 mg duas vezes ao dia). Os principais órgãos alvo para lesões não neoplásicas da pele foram a pele (hiperplasia epidérmica), o crescimento dos dentes (degeneração/atrofia do órgão do esmalte dos incisivos superiores e inflamação da gengiva/epitélio odontogênico dos incisivos) e do timo (aumento da incidência e/ou gravidade da diminuição de linfócitos).
Estudo em animais jovens
Em um estudo de desenvolvimento juvenil, Nilotinibe foi administrado via oral por gavagem a ratos jovens a partir da primeira semana após o parto até a idade adulta (70 dias após o parto) em doses de 2, 6 e 20 mg/kg/dia. Os efeitos foram limitados a dose de 20 mg/kg/dia e consistiram em reduções nos parâmetros de peso e consumo de alimento com recuperação após o fim da administração. A dose de 6 mg/kg/dia em ratos jovens não apresentou efeitos adversos. Em geral, o perfil de toxicidade nos ratos jovens foi comparável ao observado em ratos adultos.
Fototoxicidade
O Nilotinibe mostrou absorver luz nas frequências UV-A e UV-B, e ser distribuído na pele, apresentando potencial fototóxico in vitro. Entretanto, nenhuma fototoxicidade foi observada in vivo. Assim sendo, o risco do Nilotinibe causar fotossensibilização em pacientes é considerado muito baixo.

 Revisado por Isabelle Baião de Mello Neto (CRF-MG 24309)
Revisado por Isabelle Baião de Mello Neto (CRF-MG 24309)