Qual a ação da substância do Myozyme?
Resultados de eficácia
A eficácia de Alfaglicosidase foi avaliada em três estudos clínicos com pacientes que nunca haviam recebido terapia de reposição enzimática no início do tratamento e está detalhada a seguir. Além disso, diversos outros estudos e programas de acesso expandido foram realizados.
O estudo principal, AGLU01602, é um estudo clínico controlado historicamente, multicêntrico e internacional, realizado em 18 pacientes com a forma infantil da doença de Pompe, não dependentes de ventilação mecânica e com idades de sete meses ou menos na época da primeira infusão. Os pacientes foram randomizados em dois grupos, a fim de receberem 20 mg/kg ou 40 mg/kg de Alfaglicosidase a cada duas semanas, com duração de tratamento variando de 52 a 106 semanas. O resultado principal era a proporção de pacientes vivos e sem ventilação invasiva aos 18 meses de idade (período para o evento). Um grupo não tratado, derivado de um estudo retrospectivo de história natural (n = 62), serviu como grupo controle para avaliação do resultado primário. A condição cardíaca e a função motora foram avaliadas como resultados secundários.
O resultado primário de eficácia para o estudo AGLU01602 foi obtido. No marco de 18 meses, 13 dos 18 pacientes do AGLU01602 estavam vivos e sem ventilação invasiva, três estavam recebendo assistência ventilatória invasiva e dois pacientes que não tinham atingindo a idade de 18 meses ao final do estudo foram excluídos da análise, embora ainda estivessem vivos e sem a assistência ventilatória invasiva naquele momento. Os dados para o resultado primário são detalhados na Tabela 1 e na Figura 1.
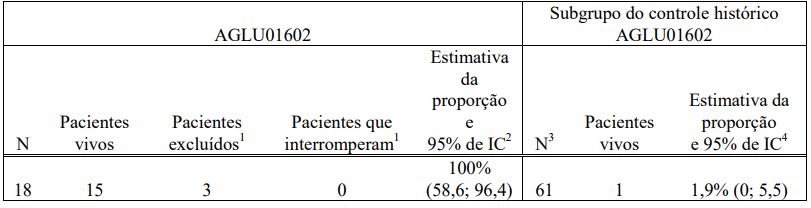
Tabela 1. Sobrevivência sem ventilador invasivo aos 18 meses no AGLU01602 e sobrevivência geral no subgrupo de controle histórico do AGLU01602

1 Os pacientes excluídos referem-se àqueles que não atingiram o limite de idade de 18 meses, mas não receberam ventilação invasiva ao final do estudo. O paciente 315 foi excluído na idade de 15,9 meses, e o paciente 318 na idade de 17,9 meses.
2 Os pacientes que interromperam são aqueles que receberam ventilação invasiva antes da idade limite.
3 As proporções são da análise de Kaplan-Meier do tempo para ventilação invasiva ou óbito.
4 Um paciente foi excluído dessa análise, já que a data da morte era desconhecida.
5 As proporções são da análise de Kaplan-Meier do tempo para óbito.
Figura 1. Estimativa de tempo de Kaplan-Meier para ventilação invasiva ou morte a partir da data de nascimento até 18 meses de idade (comparação ao subgrupo de controle histórico): AGLU01602
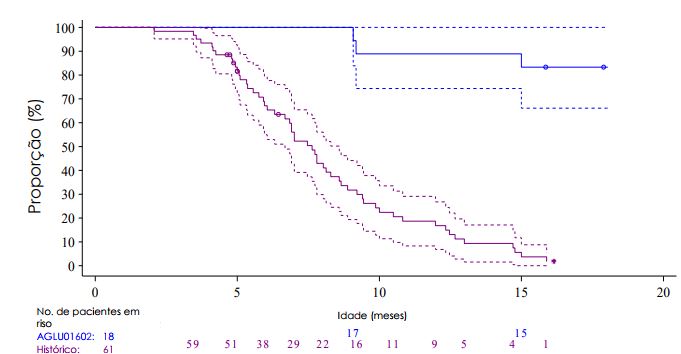
A linha em azul indica a estimativa de Kaplan-Meier da proporção dos pacientes vivos e sem a ventilação invasiva em função da idade. A linha pontilhada em azul mostra 95% de IC para esta estimativa. A linha em roxo indica a estimativa de Kaplan-Meier da proporção dos pacientes vivos em função da idade no subgrupo controle. As linhas pontilhadas roxas mostram 95% de IC para esta estimativa. Os círculos indicam as observações excluídas (pacientes 315 e 318). Três pacientes não atingiram esse resultado, uma vez que precisaram da assistência ventilatória invasiva [paciente 301, com idade de 15 meses (semana 43); paciente 319, com idade de 9,1 meses (semana 32); e paciente 317, com idade de 9,2 meses (semana 13)].
*O asterisco indica que um paciente do grupo de controle histórico permaneceu vivo aos 18 meses de idade; esse paciente morreu aos 44 meses.
O tratamento com Alfaglicosidase aumentou enormemente a sobrevivência dos pacientes, conforme avaliado aos 18 meses de idade (Tabela 2).
Tabela 2. Taxas de sobrevivência aos 18 meses no AGLU01602 e no subgrupo do controle histórico do AGLU01602
1 Os pacientes excluídos referem-se àqueles que não atingiram 18 meses de idade antes do final do estudo, mas permaneceram vivos ao final do estudo; os que interromperam referem-se aos pacientes que morreram aos 18 meses de idade.
2 A proporção é da análise de Kaplan-Meier no momento da morte; metodologia exata binomial foi utilizada para calcular 95% de IC nesse caso.
3 Um paciente foi excluído dessa análise, já que a data da morte era desconhecida.
4 Estimativa da proporção e 95% de IC com base na análise de Kaplan-Meier no momento da morte.
As alterações dos valores iniciais em relação aos do mês 12 no índice de massa do ventrículo esquerdo (IMVE) foram medidas por meio de ecocardiograma. Para os 14 pacientes que realizaram ecocardiograma inicial e na semana 52, todos apresentaram diminuições nos valores do IMVE (diminuição média de 118 g/m2 , variação de 45 a 193 g/m2 ). Treze pacientes (72%) obtiveram ganhos na função motora em relação aos valores de referência iniciais, conforme medidos por meio dos escores idade-equivalentes do desempenho motor da Escala Motora Infantil Alberta (AIMS).
Dezesseis dos 18 pacientes que participaram do Estudo AGLU01602 foram incluídos em um estudo de extensão (AGLU02403) por até 150 semanas. Um paciente morreu e não entrou no estudo de extensão. Um segundo paciente continuou o tratamento sob um programa de acesso expandido internacional. No final do estudo, 14 de 16 pacientes (87,5%) estavam vivos, e 9 de 16 pacientes (56,3%) estavam vivos e sem necessidade de assistência ventilatória invasiva. Um paciente morreu após o fim do estudo, e outro após sair do estudo.
Tabela 3: Análise do modelo de regressão de Cox: estimativa do efeito da alfa-alglicosidase sobre a sobrevida livre de ventilação invasiva, sobrevida livre de ventilação e sobrevida geral utilizando AGLU01602/AGLU02403 e pacientes de grupo de controle histórico
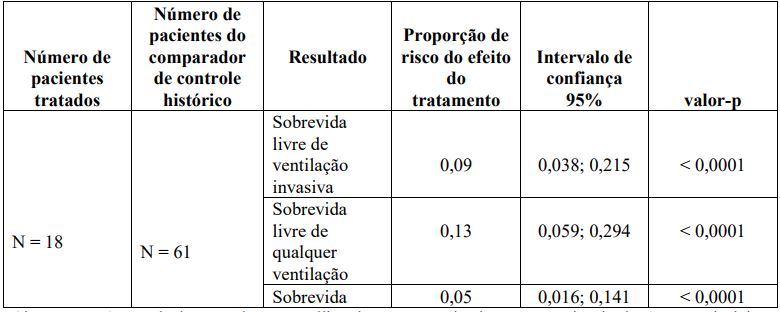
Observação: Os resultados são de uma análise de regressão de riscos proporcionais de Cox que inclui o tratamento como uma covariável dependente do tempo e também se ajusta por idade de diagnóstico e idade de início dos sintomas. Os dados até o fim do estudo AGLU02403 (12 de junho de 2006) estão incluídos nos modelos.
Na última avaliação, sete pacientes (38,9%) tiveram massa ventricular esquerda dentro dos limites normais, e a média de IMVE tinha diminuído 40%. No final do estudo de extensão, um total de onze pacientes (61%) adquiriu novas habilidades motoras com o tratamento com alfa-alglicosidase, incluindo a obtenção de deambulação independente, conforme avaliado pela AIMS e escores de marcos motores. Os sete pacientes restantes (38,9%) foram classificados como não respondedores motores no final do estudo, e tiveram habilidades motoras grossas mínimas ou não significativas. Três pacientes tiveram ganhos motores significativos durante o estudo, mas que não foram mantidos até o final.
O estudo AGLU01702 era um estudo clínico aberto, multicêntrico, internacional, com 21 pacientes com a forma infantil da doença, que tinham idades entre três meses e três anos e meio quando começaram o tratamento. Todos os pacientes receberam 20 mg/kg de Alfaglicosidase em semanas alternadas, por até 168 semanas. Cinco dos 21 pacientes estavam recebendo assistência ventilatória invasiva no momento da primeira infusão.
A medida de desfecho primário era a proporção de pacientes vivos no término do tratamento. No final do estudo, 15 dos 21 pacientes (71,4%) permaneceram vivos. Nenhuma das mortes foi avaliada como relacionada ao tratamento com Alfaglicosidase. O efeito do tratamento com Alfaglicosidase sobre a sobrevivência também foi avaliado, utilizando um modelo de risco proporcional de Cox para adequação do tempo para o evento, a partir do diagnóstico da doença. Os pacientes tratados foram comparados com os pacientes não tratados de um grupo de referência anterior. Os resultados da análise da Cox (Tabela 4) indicam que neste estudo, Alfaglicosidase reduziu o risco de morte em 79% (razão de risco 0,209), o que é também altamente significativo.
Tabela 4. Resultados sobre a sobrevivência para o estudo AGLU01702 utilizando o modelo de regressão de Cox
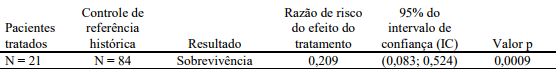
Observação: Os resultados foram obtidos a partir da análise de regressão de risco proporcional de Cox, que inclui o tratamento como uma covariável dependente do tempo, e também a idade do diagnóstico e a idade no surgimento do sintoma. A análise foi feita do momento do diagnóstico até o final do estudo (14 de julho de 2006).
Dezesseis pacientes estavam sem assistência ventilatória invasiva no momento da primeira infusão.
No final do estudo, sete (43,8%) pacientes permaneceram sem ventilação invasiva, cinco morreram e quatro ficaram dependentes de ventilação invasiva.
Quinze dos 21 pacientes (71%) apresentaram melhora na cardiomiopatia, conforme avaliados por meio de diminuição na massa ventricular esquerda da primeira à última avaliação do estudo. Dois outros pacientes mantiveram a massa do ventrículo esquerdo (MVE) normal em todo o estudo. Treze de 21 pacientes (61,9%) tiveram ganhos mensuráveis na função motora, como determinado pelos aumentos nos escores idade-equivalente a partir da linha de base na Escala AIMS e/ou Escala de Desenvolvimento Motor de Peabody. Os pacientes restantes (8 de 21, 38,9%) não demonstraram ganhos mensuráveis durante essas avaliações motoras.
O estudo AGLU02704 foi um estudo randomizado, duplo cego, placebo controlado de 90 pacientes (45 homens, 45 mulheres) com doença de Pompe de início tardio, que variaram em idade de 10 a 70 anos no início do tratamento. Todos os pacientes eram virgens em relação à terapia de reposição enzimática. Os pacientes foram randomizados na proporção 2:1 e receberam 20 mg/kg de alfaalglicosidase (n = 60) ou placebo (n = 30) em semanas alternadas, por 78 semanas (18 meses). No início do estudo, todos os pacientes eram capazes de andar (alguns exigiam dispositivos auxiliares de marcha), não necessitavam de assistência ventilatória invasiva ou ventilação não invasiva enquanto acordados e sentados, e tinham uma capacidade vital forçada (CVF) entre 30% e 79% da prevista nesta posição. Pacientes que não puderam andar 40 metros em seis minutos ou que foram incapazes de realizar teste de função pulmonar e muscular apropriado foram excluídos do estudo.
As avaliações do resultado de eficácia coprimária foram a distância caminhada em metros, em seis minutos (teste de caminhada de seis minutos 6MWT) e a CVF% prevista na posição sentada. Após 78 semanas, os pacientes tratados com alfa-alglicosidase mostraram melhora na distância caminhada, conforme medido pelo 6MWT, e na estabilização da função pulmonar, conforme medido pela CVF% prevista, em comparação à pacientes tratados com placebo.
A distância média caminhada estimada em seis minutos aumentou 25,13 metros para os pacientes que receberam alfa-alglicosidase e diminuiu 2,99 metros para os pacientes que receberam placebo, indicando um efeito estatisticamente significativo do tratamento com alfa-alglicosidase, em comparação ao placebo, de +28,12 metros (p = 0,0347). A CVF% média estimada prevista aumentou 1,20% para os pacientes tratados com alfaalglicosidase e diminuiu 2,20% para os pacientes que receberam placebo, com efeito estatisticamente significativo de 3,40% (p = 0,0055). Os resultados são mostrados na Tabela 5, abaixo:
Tabela 5: Mudança a partir da linha de base: resultados da eficácia no estudo controlado por placebo
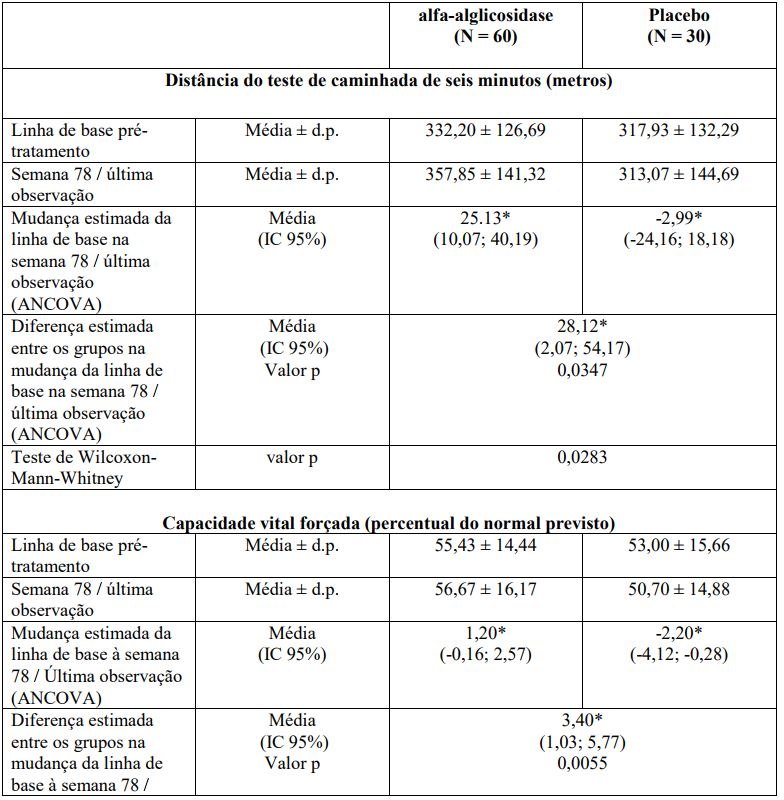
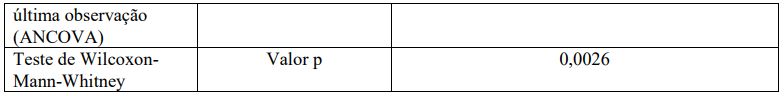
*Estimativas são baseadas na ANCOVA, ajustes para randomização strata são baseados em observação.
O AGLU02804 era um estudo clínico aberto, de centro único, que avaliou a eficácia do Alfaglicosidase em cinco pacientes da doença de Pompe de início tardio e idade variando de 5 a 15 anos no início do tratamento. Os pacientes receberam 20 mg/kg de Alfaglicosidase em semanas alternadas durante 26 semanas. Todos os pacientes eram capazes de andar e todos, exceto um, não necessitavam de qualquer forma de assistência ventilatória (um paciente necessitava de ventilação não invasiva noturna). Dos três pacientes com envolvimento pulmonar significativo na linha de base (com CVF prevista na posição sentada variando de 58 a 67%), dois demonstraram progressos clinicamente significativos na CVF (+11,5 e +16%) na posição sentada na semana 26. A avaliação da função motora foi realizada utilizando o teste de caminhada de seis minutos (6MWT). Três dos pacientes demonstraram progresso clinicamente significativo, variando de 41 a 118 metros no 6MWT em uma velocidade rápida na semana 26. Um paciente apresentou progressos no 6MWT em velocidade confortável.
Características Farmacológicas
Propriedades farmacodinâmicas
A doença de Pompe (também conhecida como deficiência de maltase ácida, doença de depósito de glicogênio Tipo II ou glicogenose Tipo II) é um transtorno hereditário do metabolismo do glicogênio, causado pela deficiência da atividade da enzima lisossômica alfa glicosidase ácida (GAA). A doença de Pompe ocorre devido ao acúmulo intralisossômico de glicogênio em vários tecidos, particularmente no músculo cardíaco e nos músculos esqueléticos, levando ao desenvolvimento de cardiomiopatia, debilidade muscular progressiva e prejuízo da função respiratória.
Alfaglicosidase representa uma fonte exógena de GAA. Alfaglicosidase se liga aos receptores de manose-6- fosfato na superfície da célula, por meio das cadeias de carboidrato da molécula e após a ligação, Alfaglicosidase é internalizado e transportado para os lisossomos, onde passa por clivagem proteolítica que resulta no aumento de sua atividade enzimática. Então, Alfaglicosidase exerce atividade enzimática de clivagem do glicogênio no lisossomo.
Propriedades farmacocinéticas
A farmacocinética de Alfaglicosidase foi avaliada em 15 pacientes no estudo principal AGLU01602, com idades variando de um mês a sete meses, durante a primeira infusão, que receberam 20 mg/kg ou 40mg/kg (como infusão aproximada de 4 a 6,5 horas) de Alfaglicosidase a cada duas semanas. A avaliação da concentração da alfa-alglicosidase no plasma foi baseada em ensaio de atividade utilizando substrato artificial. A exposição sistêmica foi aproximadamente proporcional à dose entre as doses de 20 e 40mg/kg.
Após a primeira e a sexta infusão de Alfaglicosidase, as concentrações máximas médias plasmáticas (Cmáx) variaram de 178,2 a 263,7 µg/mL para os grupos de dose de 20mg/kg e 40 mg/kg. A área média sob a curva de tempo de concentração do plasma (AUC) variou de 977,5 a 1.872,5 µgh/mL para os grupos de dose de 20mg/kg e 40mg/kg. A depuração plasmática média (CL) foi 21,9 mL/kg/h e o volume médio de distribuição no estado de equilíbrio (Vss) foi 66,2 mL/kg para ambos os grupos de dose, com uma pequena variabilidade entre os pacientes de 15% e 11%, respectivamente. A meia-vida média de eliminação (t½) foi de 2,75 horas para os dois grupos de dose.
A farmacocinética da alfa-alglicosidase também foi avaliada em 14 pacientes no estudo de apoio AGLU01702, com idades variando de seis meses a três anos e meio, durante a primeira infusão. Os pacientes receberam 20 mg/kg de Alfaglicosidase através de infusão com duração aproximada de quatro horas a cada duas semanas. Os parâmetros farmacocinéticos eram similares àqueles observados para o grupo de dose de 20 mg/kg no estudo AGLU01602.
A farmacocinética da alfa-alglicosidase foi avaliada em um estudo randomizado, duplo-cego, controlado por placebo de pacientes com início tardio da doença de Pompe, em 32 pacientes variando de 21 a 70 anos de idade, que receberam 20 mg/kg de alfa-alglicosidase em semanas alternadas. AUC e Cmáx foram similares às visitas nas semanas 0, 12 e 52, indicando que a farmacocinética de alfaalglicosidase não é dependente do tempo. Na semana 52 da administração quinzenal, as estimativas de AUC (2710 μg·h/mL), Cmáx (370 μg·h/mL) e depuração (639 mL/h) foram determinadas em estado de equilíbrio.
A depuração média mais alta (42%) foi observada na semana 52, em quatro dos cinco pacientes que foram positivos para anticorpos que inibem a captação celular da enzima em ensaio in vitro. A farmacocinética em quatro desses cinco indivíduos com o tempo indicou aumento na depuração, com aumento do título da IgG. O status de anticorpo inibitório positivo correlacionou-se aos títulos mais altos de IgG em pacientes que receberam alfa-alglicosidase. Não houve relação aparente entre a inibição de captação e a eficácia.
A farmacocinética do Alfaglicosidase foi avaliada em um estudo com cinco pacientes com doença de Pompe de início tardio com idade de cinco a quinze anos, que receberam 20 mg/kg de Alfaglicosidase a cada duas semanas. Não houve diferença no perfil farmacocinético do Alfaglicosidase nos pacientes com início tardio da doença, quando comparados aos pacientes com a forma infantil da doença.

 Revisado por Isabelle Baião de Mello Neto (CRF-MG 24309)
Revisado por Isabelle Baião de Mello Neto (CRF-MG 24309)