Qual a ação da substância do Erleada?
Resultados de Eficácia
Um total de 1207 pacientes com câncer de próstata não metastático resistente à castração (nm-CRPC) foram randomizados 2:1 para receber Apalutamida por via oral em uma dose de 240 mg ao dia em combinação com ADT (terapia de privação androgênica ou castração medicamentosa ou cirúrgica) ou placebo com ADT (terapia de privação androgênica) em um estudo clínico, multicêntrico, duplo-cego, Estudo 1 (ARN-509-003). Pacientes envolvidos apresentavam tempo de duplicação (PSADT) do Antígeno Prostático Específico (PSA) ≤ 10 meses. Na triagem, todos os pacientes foram avaliados para exclusão de metástases com cintilografia óssea com tecnécio-99m e tomografia computadorizada (TC) da pelve, abdome, tórax e crânio. Todos os pacientes que não haviam sido castrados cirurgicamente receberam ADT continuamente durante o estudo. Setenta e três por cento (73%) dos pacientes receberam tratamento anterior de anti-androgênio de primeira geração; 69% dos pacientes receberam bicalutamida e 10% dos pacientes receberam flutamida. Corticoides sistêmicos não foram permitidos na inclusão do estudo. Os resultados de PSA foram cegados e não foram utilizados para descontinuação do tratamento. Os pacientes randomizados para ambos os braços deveriam continuar o tratamento até a progressão da doença definida pela revisão cega centralizada de imagem (BICR), início de um novo tratamento, toxicidade inaceitável ou retirada do paciente do estudo. Após confirmação por BICR do desenvolvimento de doença metastática à distância, os pacientes receberam como opção acetato de abiraterona para o primeiro tratamento subsequente após a descontinuação do tratamento no estudo.
As seguintes características demográficas e características basais da doença foram equilibradas entre os braços do tratamento. A mediana de idade foi de 74 anos (intervalo 48-97) e 26% dos pacientes tinham 80 anos de idade ou mais. A distribuição racial foi 66% caucasiana, 5,6% negra, 12% asiática e 0,2% outra. Setenta e sete por cento (77%) dos pacientes em ambos os braços de tratamento teve cirurgia prévia ou radioterapia da próstata. A maioria dos pacientes apresentava uma pontuação Gleason de 7 ou superior (81%). Quinze por cento (15%) dos pacientes tinham linfonodos pélvicos < 2 cm na entrada no estudo. Todos os indivíduos envolvidos foram confirmados como não metastáticos por revisão centralizada cega de imagem e tinham um “performance status ECOG” (Eastern Cooperative Oncology Group) de 0 ou 1 no início do estudo.
A sobrevida livre de metástase (MFS) é definida como o tempo desde a randomização até o momento da primeira evidência de metástase óssea ou de partes moles à distância confirmado pelo BICR ou morte devido a qualquer causa, o que ocorrer primeiro. O tratamento com Apalutamida aumentou significativamente o MFS. Apalutamida diminuiu o risco de metástase à distância ou morte em 72%. A mediana de sobrevida livre de metástase para Apalutamida foi de 41 meses e foi de 16 meses para o placebo.
Figura 1: Curva de Kaplan-Meier de sobrevida livre de metástase (MFS) no estudo 1
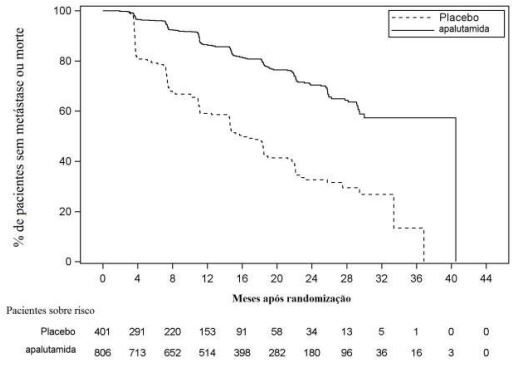
Figura 2: Sobrevida livre de metástases por subgrupos no estudo 1
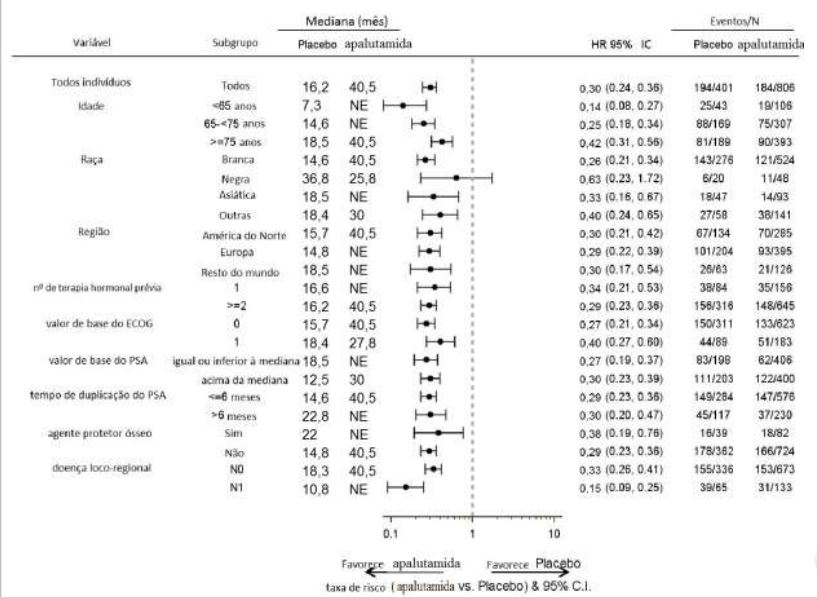
Todos indivíduos = população de intenção de tratamento.
A análise não estratificada é apresentada na Figura 2.
Os indivíduos tratados com Apalutamida e ADT mostraram melhora significativa em relação aos tratados apenas com ADT para os seguintes desfechos secundários: tempo para metástases (TTM), sobrevida livre de progressão (PFS) e tempo para progressão sintomática. Além disso, a sobrevida global (OS) e o tempo para início da quimioterapia citotóxica também foram melhorados.
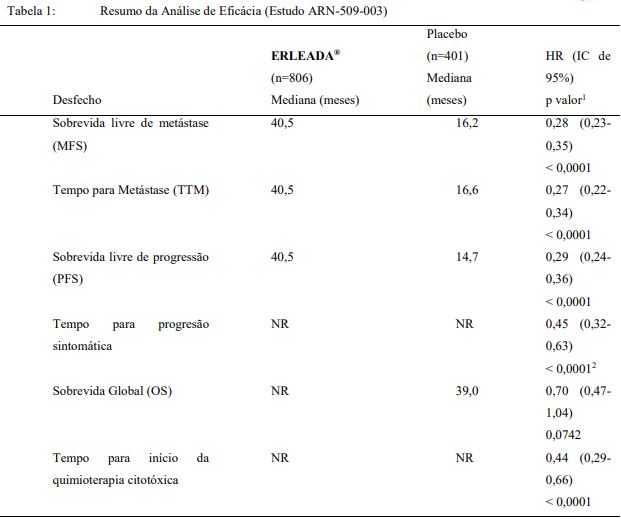 NR = Não alcançado.
NR = Não alcançado.
1 p valor do teste log-rank estratificado.
2 Valor p real – 0,00000356; portanto, o limite de eficácia do tipo OBF de 0,00008 é cruzado na avaliação interina de progressão sintomática.
O tratamento com Apalutamida diminuiu significativamente o risco de progressão sintomática em 55% em comparação com o placebo. O valor de p observado (0,00000356) cruzou o limite de eficácia de Obrien-Fleming (OBF) (p = 0,00008) para significância.
Figura 3: Gráfico de Kaplan-Meier de tempo para progressão sintomática; População de intenção de tratamento no Estudo 1
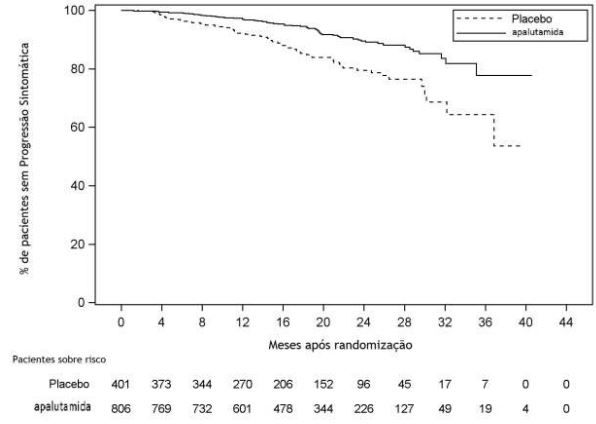
A sobrevida global foi maior para Apalutamida do que para placebo com uma relação de risco (HR) de 0,700 (IC de 95%: 0,472-1,038). O valor de p foi 0,0742 que não atingiu o valor pré-especificado para significância estatística. Trinta e nove por cento (39%) dos indivíduos tratados com Apalutamida e 70% dos indivíduos tratados com placebo descontinuaram o tratamento no estudo. Uma maior proporção (80%) dos indivíduos tratados com placebo recebeu terapia subsequente em comparação com indivíduos tratados com Apalutamida (56%). A Sobrevida livre de progressão secundária (PFS-2, definida como o tempo até a progressão da doença após a primeira terapia subsequente ou morte) foi maior para os indivíduos tratados com Apalutamida em relação aos tratados com placebo (HR = 0,489; IC de 95%: 0,361-0,662; p <0,0001).
Características Farmacológicas
Propriedades farmacodinâmicas
Mecanismo de ação
A Apalutamida é um inibidor seletivo de receptor de androgênio (AR), administrado por via oral, que se liga diretamente ao domínio de ligação do AR. A Apalutamida impede a translocação nuclear do AR, inibe a ligação no DNA, impede a transcrição mediada por AR e não possui atividade agonista do receptor androgênico em estudos pré-clínicos. Em modelos de ratos com câncer de próstata, a administração de Apalutamida causa diminuição da proliferação de células tumorais e aumento da apoptose levando a uma potente atividade antitumoral. O principal metabolito, a N-desmetil-apalutamida, exibiu um terço da atividade in vitro da Apalutamida.
Efeitos farmacodinâmicos
Efeito no intervalo QT / QTc e eletrofisiologia cardíaca O efeito da Apalutamida 240 mg uma vez ao dia no intervalo QT foi avaliado em indivíduos com CPRC em um estudo QT dedicado. Não houve diferença maior que 20 ms na variação média do intervalo QT a partir da linha de base, com base no método de correção Fridericia, em todos os pontos no estado de equilíbrio.
Propriedades farmacocinéticas
Após a repetição das doses diárias, a exposição à Apalutamida (Cmax e área sob a curva [ASC]) aumentou de forma proporcional à dose em toda a faixa de doses de 30 a 480 mg. Após a administração de 240 mg uma vez por dia, o estado de equilíbrio de Apalutamida foi alcançado após 4 semanas e a proporção média de acumulação foi aproximadamente 5 vezes em relação a uma dose única. No estado de equilíbrio, os valores médios (CV%) Cmax e ASC para a Apalutamida foram de 6 μg/mL (28%) e 100 μg.h/mL (32%), respectivamente. As flutuações diárias nas concentrações plasmáticas de Apalutamida foram baixas, com uma relação média entre de pico até vale de 1,63. Foi observado um aumento na depuração aparente (CL/F) com dose repetida, provavelmente devido à indução do próprio metabolismo da Apalutamida.
No estado de equilíbrio, os valores médios (CV%) Cmax e ASC para o principal metabolito ativo, N-desmetilapalutamida, foram de 5,9 μg/mL (18%) e 124 μg.h/mL (19%), respectivamente. N-desmetil-apalutamida é caracterizada por um perfil de concentração plana no tempo no estado de equilíbrio com uma relação média de pico até o vale de 1,27. A proporção média (CV%) do metabolito de ASC/fármaco-mãe para N-desmetil-apalutamida após administração de dose repetida foi de cerca de 1,3 (21%). Com base na exposição sistêmica, a potência relativa e as propriedades farmacocinéticas, a N-desmetil-apalutamida provavelmente contribuiu para a atividade clínica da Apalutamida.
Absorção
Após a administração oral, o tempo médio para atingir a concentração plasmática máxima (tmax) foi de 2 horas (intervalo: 1 a 5 horas). A biodisponibilidade oral média absoluta é de aproximadamente 100%, indicando que a Apalutamida é completamente absorvida após a administração oral.
A administração de Apalutamida em indivíduos saudáveis em condições de jejum e após uma refeição rica em gordura não resultou em mudanças clinicamente relevantes no Cmax e ASC. O tempo mediano para atingir tmax foi atrasado cerca de 2 horas com alimentos.
Distribuição
O volume aparente médio de distribuição no estado de equilíbrio da Apalutamida é de cerca de 276 L. O volume de distribuição da Apalutamida é maior do que o volume da água corporal total, indicando uma distribuição extravascular extensiva.
A Apalutamida e a N-desmetil-apalutamida são 96% e 95% ligadas a proteínas plasmáticas, respectivamente, e principalmente ligam-se a albumina sérica independente da concentração.
Metabolismo
Após administração oral única de 240 mg de Apalutamida marcada com 14C, a Apalutamida, o metabolito ativo, a N-desmetil-apalutamida e um metabólito de ácido carboxílico inativo representaram a maioria da 14C-radioatividade no plasma, representando 45%, 44% e 3%, respectivamente, do total 14C-AUC.
O metabolismo é a principal via de eliminação da Apalutamida. É metabolizado principalmente por CYP2C8 e CYP3A4 para formar N-desmetil-apalutamida. A apalutamide e a N-desmetil-apalutamida são ainda metabolizados para formar o metabólito de ácido carboxílico inativo pela carboxilesterase. A contribuição de CYP2C8 e CYP3A4 no metabolismo da Apalutamida é estimada em 58% e 13% após a dose única, mas muda para 40% e 37%, respectivamente, no estado de equilíbrio.
Eliminação
A Apalutamida, principalmente sob a forma de metabólitos, é eliminada principalmente através da urina. Após uma única administração oral de Apalutamida radiomarcada, 89% da radioatividade foi recuperada até 70 dias após a dose: 65% foi recuperado na urina (1,2% da dose como Apalutamida inalterada e 2,7% como N-desmetilApalutamida) e 24% foi recuperado nas fezes (1,5% de dose como Apalutamida inalterada e 2% como N-desmetil-apalutamida).
O CL/F da Apalutamida é 1,3 L/h após administração única e aumenta para 2,0 L/h no estado de equilíbrio após uma dose única diária. A meia-vida efetiva média para a Apalutamida em indivíduos é de cerca de 3 dias no estado de equilíbrio.
População especial
Os efeitos da insuficiência renal, insuficiência hepática, idade, raça e outros fatores extrínsecos na farmacocinética da Apalutamida estão resumidos na Figura 4.
Figura 4: Efeitos de fatores intrínsecos/extrínsecos e outros medicamentos em Apalutamida
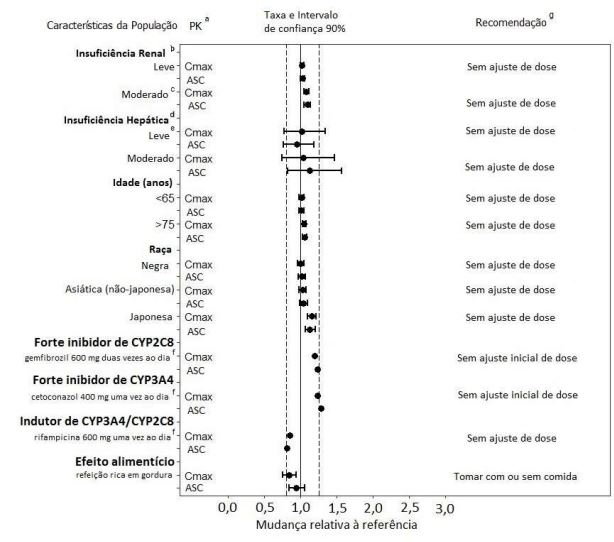
a Os parâmetros de Farmacocinética (PK) (Cmax e ASC) são para a Apalutamida, exceto nos estudos de interação do fármaco, onde são para porções ativas (isto é, Apalutamida não ligada + N-desmetil-apalutamida não ligada ajustada a potência).
b O grau de insuficiência renal foi determinado com base em eGFR utilizando a equação do estudo da modificação da dieta na doença renal (MDRD); normal (≥90 mL/ min/1,73m2 ), leve (60-89 mL/min/1,73m2 ), moderada (30-59 mL/min /1,73m2 ).
c Os dados incluíram 2 indivíduos com insuficiência renal grave (≤ 29 mL/min/1,73m2 ).
d O grau de comprometimento hepático foi determinado com base na classificação Child-Pugh; leve (Child-Pugh A), moderado (Child-Pugh B).
e Uma análise de PK da população demonstrou que a insuficiência hepática leve (com base nos critérios do Instituto Nacional do Câncer) não influencia a exposição da Apalutamida.
f Efeitos na PK no estado de equilíbrio de porções ativas com base em simulações
Não foram observadas diferenças clinicamente significativas na farmacocinética da Apalutamida e da N-desmethyl apalutamide em indivíduos com insuficiência renal leve (eGFR 60-89 mL/min/1,73m2 ) ou moderada (eGFR 30-59 mL/min/1,73m2 ), insuficiência hepática leve (Child-Pugh A) ou moderada (Child-Pugh B), idade variando de 18 a 94 anos ou entre diferentes raças.
O efeito potencial de insuficiência renal grave ou doença renal terminal (eGFR ≤ 29 mL/min/1,73m2 ) não foi estabelecido devido a dados insuficientes. Os dados clínicos e farmacocinéticos não estão disponíveis para pacientes com insuficiência hepática grave (Child-Pugh Classe C).

 Revisado por Isabelle Baião de Mello Neto (CRF-MG 24309)
Revisado por Isabelle Baião de Mello Neto (CRF-MG 24309)