Como o Bozemyb funciona?
Resultados de eficácia
Estudo em pacientes não tratados
Estudo Fase 3 comparando combinação terapêutica versus tratamento padrão em 682 pacientes não candidatos a transplante.
Tabela 1: Características iniciais dos pacientes
Característica | Grupo VMP | Grupo MP |
Idade mediana (anos) | 71,0 | 71,0 |
Tabela 2: Resumo de eficácia
Desfecho | VMP | MP |
Tempo até progressão | ||
Mediana (meses) | 20,7 | 15,0 |
Pacientes elegíveis a transplante
Três estudos Fase 3 (1572 pacientes) demonstraram benefícios em sobrevida livre de progressão e taxas de resposta.
Tabela 3: Resultados com tratamento de indução contendo Bortezomibe (Vc)
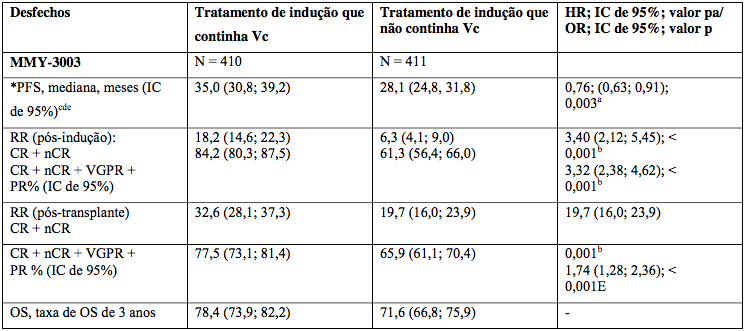
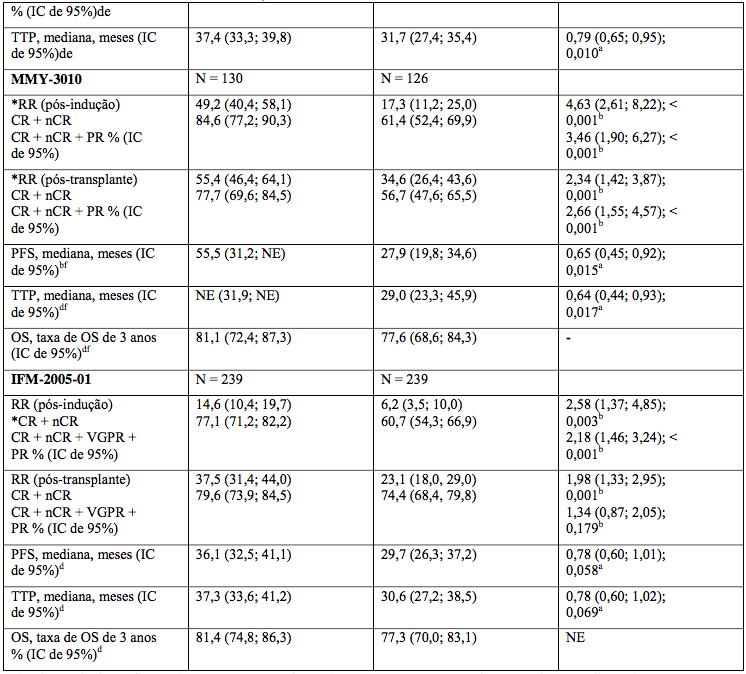
Estudos em mieloma recorrente
Estudo Fase 3 comparando com dexametasona em 669 pacientes. Grupo com Bozemyb apresentou maior taxa de resposta (38% vs 18%) e maior tempo até progressão (6,2 vs 3,5 meses).
Tabela 7: Resumo de eficácia
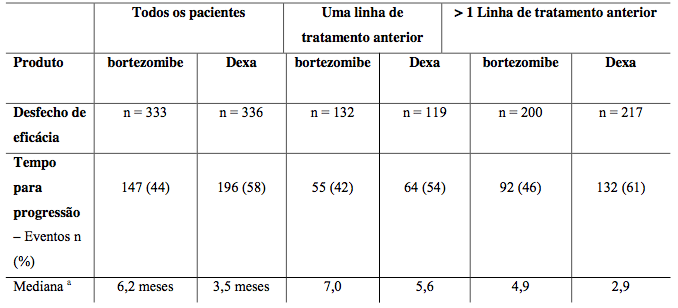
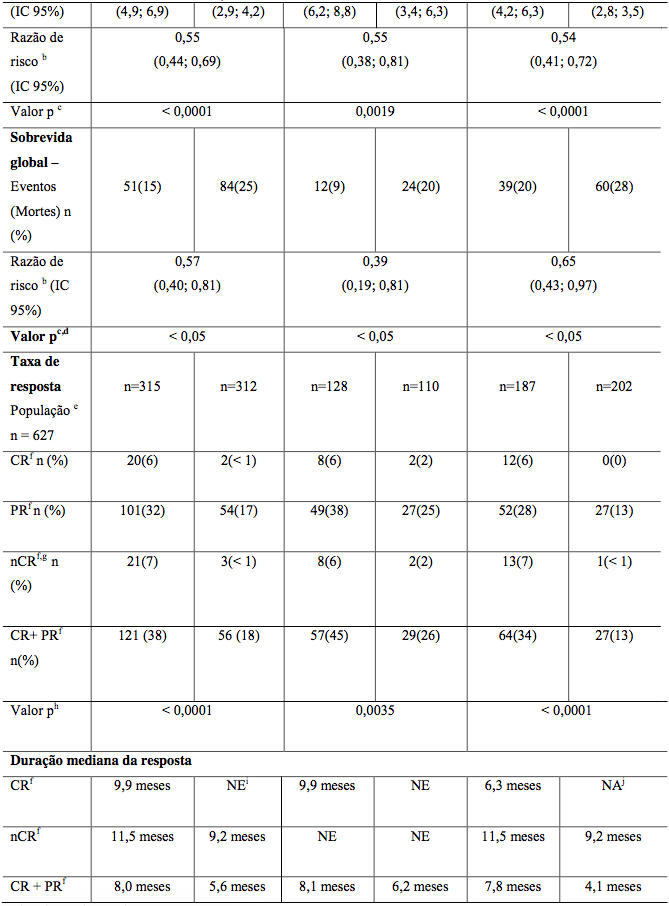
Estudo comparando aplicação na veia versus sob a pele
Estudo mostrou equivalência entre vias subcutânea e intravenosa. Taxa de resposta similar (42% em ambos).
Tabela 9: Resumo de eficácia por via de aplicação
Via Veia (IV) | Via Pele (SC) | |
Taxa resposta (4 ciclos) | 42% | 42% |
Características farmacológicas
Mecanismo de ação
Inibe reversivelmente o proteassoma 26S, interrompendo processos celulares essenciais e levando à morte de células cancerosas.
Farmacocinética
Após dose intravenosa de 1,3 mg/m2, concentração plasmática máxima média de 112 ng/mL. Meia-vida de eliminação entre 40-193 horas.
Exposição sistêmica equivalente entre vias subcutânea e intravenosa. Concentração máxima menor via subcutânea (20,4 vs 223 ng/mL).
Distribuição
Amplamente distribuído nos tecidos. Ligação a proteínas plasmáticas: 83%.
Metabolismo
Metabolizado principalmente por enzimas CYP3A4, CYP2C19 e CYP1A2. Metabólitos inativos.
Eliminação
Vias de eliminação não caracterizadas em humanos.
Grupos especiais
Idade, sexo e raça
Sem diferenças clinicamente relevantes. Depuração em crianças similar à adultos quando ajustada por área corporal.
Problemas hepáticos
Exposição aumentada em 60% em insuficiência moderada/grave. Use doses iniciais reduzidas e monitore.
Problemas renais
Sem alterações significativas na farmacocinética. Administrar após diálise.

 Revisado por Isabelle Baião de Mello Neto (CRF-MG 24309)
Revisado por Isabelle Baião de Mello Neto (CRF-MG 24309)