Como o Azacitidina Natcofarma do Brasil age no organismo?
Eficácia comprovada
Estudos clínicos
Estudo comparou segurança e eficácia da Azacitidina subcutânea + tratamento de suporte versus apenas tratamento de suporte em pacientes com síndromes mielodisplásicas (SMD). Pacientes com anemia refratária foram incluídos se necessitassem de transfusões ou apresentassem plaquetas baixas/neutropenia com infecções.
Azacitidina foi administrada em dose inicial subcutânea de 75 mg/m² diariamente por sete dias a cada quatro semanas, com possível aumento para 100 mg/m² após dois ciclos sem benefício. O objetivo primário foi taxa de resposta.
Dos 191 pacientes, 19 tinham diagnóstico de leucemia mielóide aguda (LMA) no início e foram excluídos da análise primária. Cerca de 55% dos pacientes do grupo controle mudaram para Azacitidina.
Tabela 1. Dados Demográficos Basais e Características da Doença:
| Azacitidina (N = 99) | Observação (N = 92) | |
| Sexo (n%) | ||
| Masculino | 72 (72,1) | 60 (65,2) |
| Feminino | 27 (27,3) | 32 (34,8) |
| Raça | ||
| Branca | 93 (93,9) | 85 (92,4) |
| Negra | 1 (1,0) | 1 (1,1) |
| Hispânica | 3 (3,0) | 5 (5,4) |
| Asiática/oriental | 2 (2,0) | 1 (1,1) |
| Idade (anos) | ||
| N | 99 | 91 |
| Média ± DP | 67,3 ±10,39 | 68,0 ± 10,23 |
| Faixa | 31-92 | 35-88 |
| Diagnóstico de SMD adjudicada na entrada do estudo (n%) | ||
| AR | 21 (21,2) | 18 (19,6) |
| ARSA | 6 (6,1) | 5 (5,4) |
| AREB | 38 (38,4) | 39 (42,4) |
| AREB-T | 16 (16,2) | 14 (15,2) |
| LMMoC | 8 (8,1) | 7 (7,6) |
| LMA | 10 (10,1) | 9 (9,8) |
| Produto para transfusão utilizado em 3 meses antes da entrada no estudo (n%) | ||
| Qualquer produto de transfusão | 70 (70,1) | 59 (64,1) |
| Células sanguíneas humanas concentradas | 66 (66,7) | 55 (59,8) |
| Plaquetas, sangue humano | 15 (15,2) | 12 (13,0) |
| Hetamido | 0 (0,0) | 1 (1,1) |
| Fração de proteína plasmática | 1 (1,0) | 0 (0,0) |
| Outros | 2 (2,0) | 2 (2,2) |
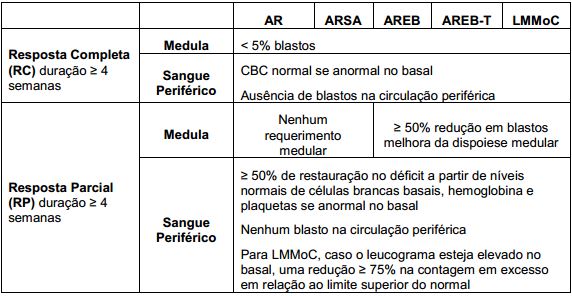
Tabela 2. Critérios de Respostas:
Taxa de resposta global de 15,7% com Azacitidina foi significativamente maior que 0% no grupo controle (p<0,0001). A maioria dos respondedores apresentava múltiplas anormalidades celulares iniciais. Pacientes dependentes de transfusão tornaram-se independentes durante resposta.
Tabela 3. Taxas de Resposta:
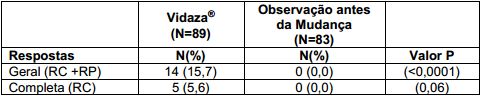

Pacientes do grupo controle que migraram para Azacitidina tiveram taxa de resposta de 12,8%.
Estudo 2
Estudo aberto com 72 pacientes mostrou taxa de resposta de 13,9%. Duração mediana da resposta foi 430 dias.
Estudo 3
Estudo com 48 pacientes mostrou taxa de resposta de 18,8% com duração mediana de 281 dias. Benefícios também foram observados em pacientes com melhora clínica sem preencher critérios completos de resposta.
Estudo internacional comparou Azacitidina + melhor cuidado de apoio versus tratamentos convencionais. Pacientes tratados com Azacitidina tiveram sobrevida mediana de 24,5 meses versus 15 meses (p=0,0001).
Curva de Kaplan-Meier de tempo de óbito por qualquer motivo (população com intenção de tratamento):
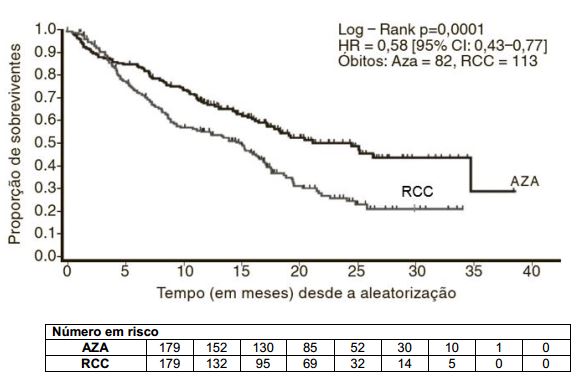
AZA = azacitidina.
RCC = regimes de cuidados convencionais.
IC = intervalo de confiança.
IR = índice de risco.
Azacitidina reduziu necessidade de transfusões de hemácias:
Tabela 4. Efeito da azacitidina em transfusões de hemácias em pacientes com SMD:
| Parâmetro de eficácia | Azacitidina MCA (n=179) | Regimes de cuidados convencionais (n=179) |
| Pacientes dependentes de transfusão que se tornaram independentes durante tratamento¹ | 50/111(45,0%) (95% IC: 35,6%, 54,8%) | 13/114 (11,4%) (95% IC: 6,2%, 18,7%) |
| Pacientes independentes que se tornaram dependentes durante tratamento | 10/68 (14,7%) (95% IC: 7,3%, 25,4%) | 28/65 (43,1%) (95% IC: 30,9%, 56,0%) |
1Independência definida como nenhuma transfusão por 56+ dias consecutivos.
Como o medicamento age no corpo?
Ação do medicamento
Como funciona
Age promovendo hipometilação do DNA em células doentes da medula óssea, restaurando funções de genes importantes. Elimina células de multiplicação rápida através de efeito citotóxico.
Processo no corpo (farmacocinética)
Após aplicação subcutânea, pico plasmático ocorre em 0,5h. Biodisponibilidade é 89% comparada à via intravenosa. Volume de distribuição médio é 76L. Eliminado principalmente pela urina (85% da dose).

 Revisado por Isabelle Baião de Mello Neto (CRF-MG 24309)
Revisado por Isabelle Baião de Mello Neto (CRF-MG 24309)