Qual a ação da substância do Vimizim?
Resultados de Eficácia
Os estudos clínicos realizados com Alfaelosulfase avaliaram o impacto do tratamento nas manifestações sistêmicas da MPS IVA em vários domínios, incluindo resistência física, função respiratória, velocidade de crescimento e mobilidade, bem como sulfato de queratano (SQ) na urina.
Um total de 235 pacientes com MPS IVA foi inscrito e exposto a Alfaelosulfase em seis estudos clínicos.
A segurança e a eficácia de Alfaelosulfase foram avaliadas em um estudo clínico randomizado, duplo-cego, controlado por placebo, de fase 3 que incluiu 176 pacientes com MPS IVA, com idades entre 5 e 57 anos. A maioria dos pacientes apresentava baixa estatura, resistência física debilitada e sintomas musculoesqueléticos. Os pacientes que conseguiam caminhar mais de 30 metros (m) e menos de 325 m em um Teste de Caminhada de 6 Minutos (TC 6) no início do estudo foram inscritos no estudo.
Os pacientes receberam Alfaelosulfase 2 mg/kg semanalmente (n=58) ou 2 mg/kg a cada duas semanas (n=59) ou placebo (n=59) durante um total de 24 semanas. Todos os pacientes foram tratados com anti-histamínicos antes de cada infusão. O desfecho primário foi a mudança, desde o início do estudo, na distância do TC 6 comparado ao placebo na Semana 24. Os desfechos secundários foram a mudança, desde o início do estudo, no Teste de Escada (TE) de 3 minutos e nos níveis de SQ na urina na Semana 24. Um total de 173 pacientes foi inscrito posteriormente em um estudo de extensão no qual os pacientes recebiam 2 mg/kg de Alfaelosulfase semanalmente ou 2 mg/kg a cada duas semanas, e depois foram migrados para 2 mg/kg a cada semana sob disponibilidade dos resultados da Semana 24.
Os desfechos primários e secundários foram avaliados na Semana 24. O efeito do tratamento observado na distância percorrida em 6 minutos de caminhada, comparado ao placebo, foi de 22,5 m (CI95, 4,0, 40,9. p=0,0174) no regime de 2 mg/kg/semana. O efeito do tratamento observado na subida de escada por minuto, comparado ao placebo, foi de 1,1 degrau/min (CI95, -2,1, 4,4. p=0,4935) no regime de 2 mg/kg/semana.
O efeito do tratamento observado no percentual de alteração no SQ na urina, comparado ao placebo, foi de -40,7% (CI95, -49,0, - 32,4. p<0,0001) no regime de 2 mg/kg/semana. A diferença foi maior entre o grupo de placebo e o grupo de tratamento semanal em todos os desfechos. Os resultados do regime a cada duas semanas na distância percorrida em 6 minutos de caminhada ou nos degraus de escada por minuto foram comparáveis ao placebo.
Tabela 1: Resultados do estudo clínico controlado por placebo de 2 mg por kg por semana
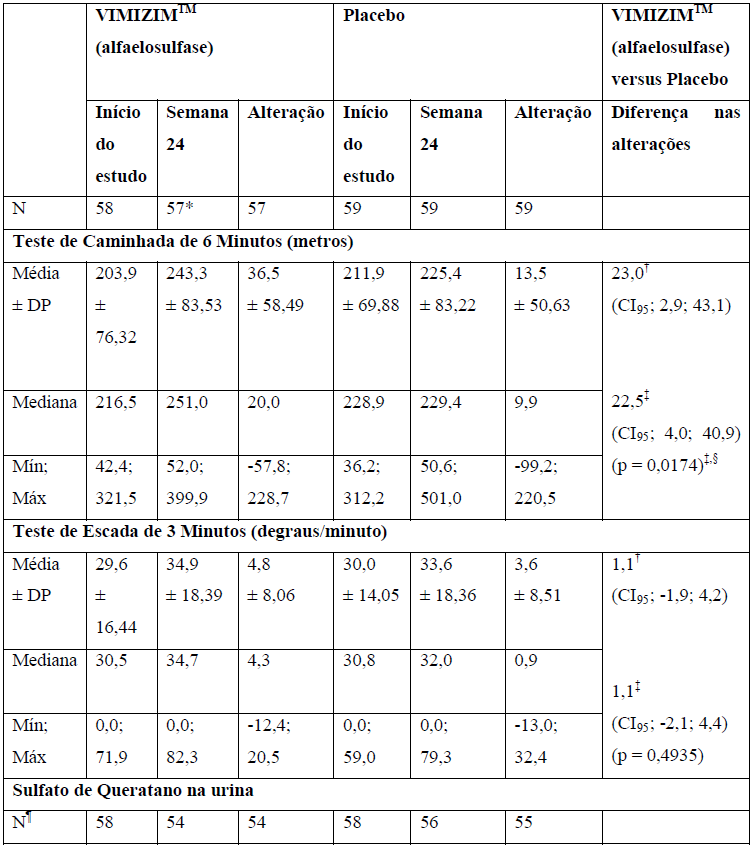
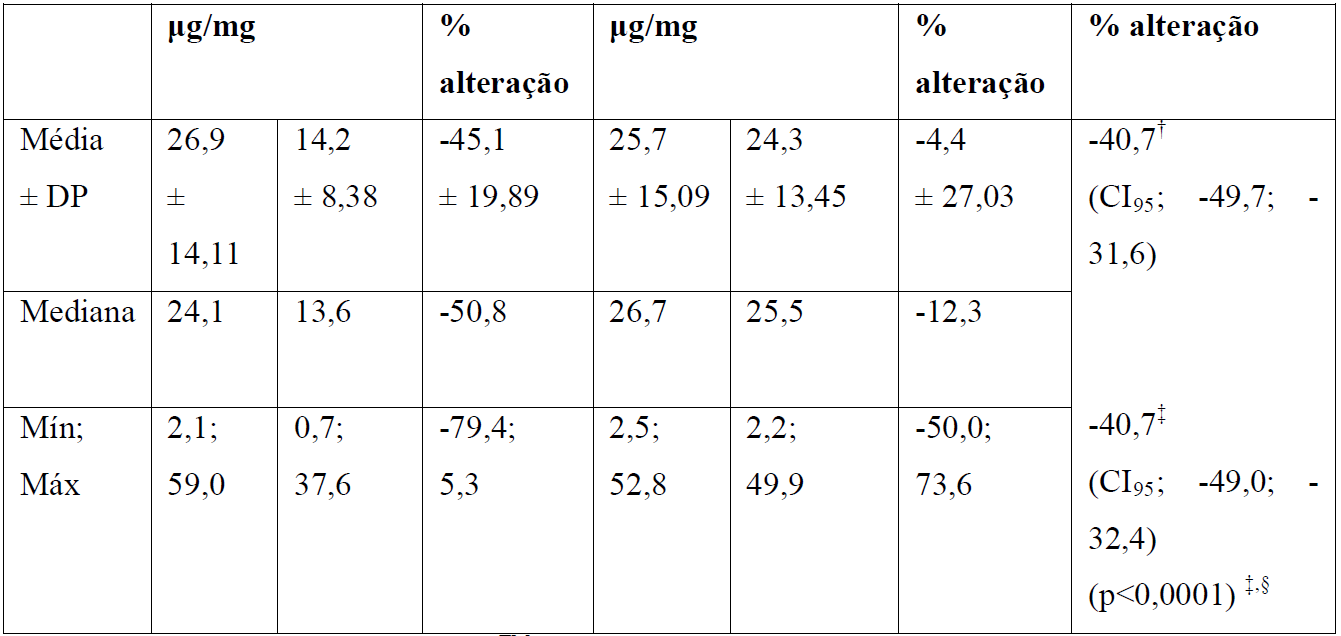
* Um paciente no grupo de Alfaelosulfase desistiu após uma infusão.
† Média observada de Alfaelosulfase – Placebo.
‡ Média baseada no modelo de Alfaelosulfase - Placebo, ajustado para o início do estudo.
§ Valor p baseado na diferença média com base no modelo.
¶ Resultados não disponíveis de todos os pacientes inscritos.
Figura 1: Alteração média nas medições ANCOVA repetidas no teste de caminhada de 6 minutos (população selecionada para tratamento)
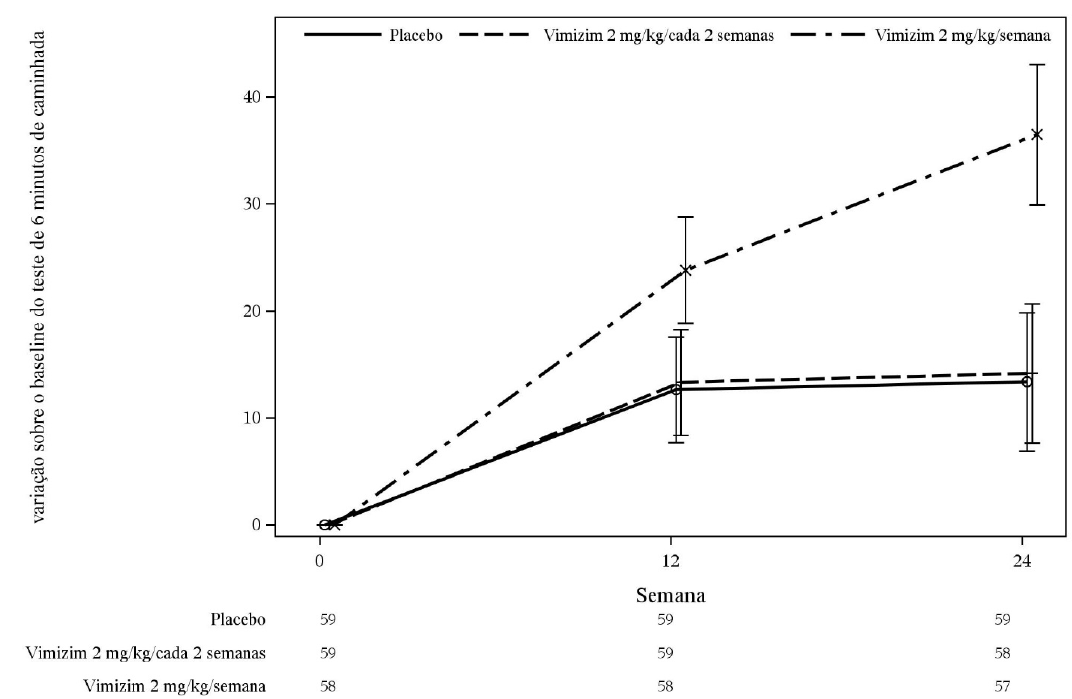
As barras de erro representam o desvio padrão da alteração média dos mínimos quadrados desde o início do estudo.
Nos estudos de extensão, os pacientes que receberam Alfaelosulfase 2 mg/kg semanalmente mostraram manutenção da melhoria inicial na resistência e permanência na redução de SQ na urina até 156 semanas.
Em um estudo aberto, 15 pacientes pediátricos com MPS IVA com menos de 5 anos de idade (9 meses a < 5 anos) receberam 2 mg/kg de Alfaelosulfase uma vez por semana por 52 semanas. Os pacientes neste estudo demonstraram uma redução na média de SQ normalizado na urina. Os resultados de segurança e de farmacodinâmica nestes pacientes foram consistentes com os resultados observados em pacientes de 5 a 57 anos de idade.
Características Farmacológicas
Mecanismo de ação
As mucopolissacaridoses abrangem um grupo de distúrbios de armazenamento lisossômico causados pela deficiência de enzimas lisossômicas específicas necessárias para o catabolismo de glicosaminoglicanos (GAG). A MPS IVA é caracterizada pela falta ou pela redução acentuada na atividade da N-acetilgalactosamina-6-sulfatase. A deficiência na atividade da sulfatase resulta no acúmulo de substratos de GAG, SQ e de sulfato de condroitina-6 (SC6) no compartimento lisossômico das células em todo o corpo. O acúmulo leva à disfunção generalizada de células, tecidos e órgãos. Alfaelosulfase destina-se a fornecer a enzima exógena N-acetilgalactosamina-6-sulfatase que entraria nos lisossomos e aumentaria o catabolismo do SQ e SC6 (GAGs). A absorção da Alfaelosulfase pelas células nos lisossomos é provavelmente mediada pela ligação de cadeias de oligossacarídeos terminadas em manose-6-fosfato da Alfaelosulfase para seus receptores.
Na falta de um modelo animal da doença, a atividade farmacológica de Alfaelosulfase foi confirmada usando condrócitos primários humanos de um paciente com MPS IVA. O tratamento de condrócitos na MPS IVA com Alfaelosulfase induziu a depuração (clearance) de armazenamento lisossômico de SQ dos condrócitos e restaurou a expressão de alguns genes condrogênicos. O SQ extracelular não foi afetado pelo tratamento com Alfaelosulfase, demonstrando que a atividade de Alfaelosulfase foi restrita ao lisossomo.
Farmacodinâmica
O efeito farmacodinâmico de Alfaelosulfase foi avaliado por reduções nos níveis de SQ na urina. A relação de SQ na urina com outras medições de resposta clínica não foi estabelecida. Nenhuma associação foi observada entre o desenvolvimento de anticorpos e os níveis de SQ na urina.
Propriedades farmacocinéticas
Os parâmetros farmacocinéticos de Alfaelosulfase foram avaliados em 23 pacientes com MPS IVA que receberam infusões intravenosas semanais de 2 mg/kg de Alfaelosulfase por aproximadamente 4 horas durante 22 semanas. Os parâmetros farmacocinéticos na Semana 0 e na Semana 22 são apresentados na Tabela 2. Na Semana 22, a AUC0-t média e a Cmáx aumentaram de 181% para 192%, respectivamente, quando comparado à Semana 0. A meia-vida média (t1/2) aumentou de 7,52 min na Semana 0 para 35,9 min na Semana 22. Pacientes do sexo masculino e feminino tiveram depuração (clearance) comparável de Alfaelosulfase, e a depuração (clearance) não variou com idade ou peso na Semana 22. Foi avaliado o impacto dos anticorpos na farmacocinética de Alfaelosulfase. Nenhuma associação foi aparente entre a titulação total de anticorpos e a depuração (clearance) de Alfaelosulfase. Entretanto, os pacientes tratados com Alfaelosulfase 2 mg/kg semanalmente, com respostas positivas de anticorpos neutralizadores, tiveram valores diminuídos de depuração (clearance) total (CL) e t1/2 prolongada. Apesar da alteração do perfil farmacocinético, a presença de anticorpos neutralizadores não afetou a farmacodinâmica, a eficácia e a segurança nos pacientes tratados com Alfaelosulfase. Nenhum acúmulo de Alfaelosulfase no plasma foi evidente após a dosagem semanal.
Tabela 2: Parâmetros de farmacocinética
Parâmetro Farmacocinético | Semana 0 Média (DP) | Semana 22 Média (DP) |
AUC0-t, mín x μg/mL* | 238 (100) | 577 (416) |
Cmáx, μg/mL† | 1,49 (0,534) | 4,04 (3,24) |
CL, mL/min/kg‡ | 10,0 (3,73) | 7,08 (13,0) |
Vdss, mL/kg§ | 396 (316) | 650 (1842) |
Vdz, mL/kg¶ | 124 (144) | 300 (543) |
t1/2, min# | 7,52 (5,48) | 35,9 (21,5) |
Tmáx, minÞ | 172 (75,3) | 202 (90,8) |
* AUC0-t, área sob a curva de concentração-tempo no plasma do tempo zero ao tempo da última concentração mensurável.
† Cmáx, concentração máxima observada no plasma.
‡ CL, depuração (clearance) total do medicamento após administração intravenosa.
§ Vdss, volume aparente de distribuição em estado de equilíbrio.
¶ Vdz, volume aparente de distribuição com base na fase terminal.
# t1/2 , meia-vida de eliminação.
Þ Tmáx, tempo de zero à concentração máxima no plasma.
Toxicologia
Dados pré-clínicos não revelaram nenhum risco especial a humanos com base nos estudos convencionais de farmacologia de segurança que avaliaram os sistemas nervoso central, respiratório e cardiovascular, toxicidade de dose única e repetida em ratos e macacos ou fertilidade e desenvolvimento embriofetal em ratos ou coelhos. Um estudo de desenvolvimento peri e pós-natal em ratos não mostrou nenhuma evidência de quaisquer efeitos no desenvolvimento pré e pós-natal em doses de até 20 mg/kg.
Carcinogênese, mutagênese e comprometimento da fertilidade
Estudos de longo prazo em animais para avaliar o potencial carcinogênico ou estudos para avaliar o potencial mutagênico não foram realizados com Alfaelosulfase. Estudos de reprodução foram realizados em ratos em doses até 10 vezes a dose humana e não revelaram nenhuma evidência de fertilidade ou desempenho reprodutivo deficientes.

 Revisado por Isabelle Baião de Mello Neto (CRF-MG 24309)
Revisado por Isabelle Baião de Mello Neto (CRF-MG 24309)