Qual a ação da substância do Luxturna?
Resultados da Eficácia
Estudos clínicos
Estudo 301
A eficácia de Voretigeno Neparvoveque em pacientes pediátricos e adultos foi avaliada em um ensaio aberto, randomizado, de dois centros (Estudo 301).
Dos 31 participantes incluídos, 21 participantes foram randomizados para receber injeção subretiniana de Voretigeno Neparvoveque. Um participante descontinuou o estudo antes do tratamento. Dez participantes foram randomizados para o grupo de controle (não intervenção). Um participante do grupo de controle retirou o consentimento e foi descontinuado do estudo. Os nove participantes que foram randomizados para o grupo de controle foram cruzados para receber injeção subretiniana de Voretigeno Neparvoveque após um ano de observação. A média de idade dos 31 participantes randomizados foi de 15 anos (faixa de 4 a 44 anos), incluindo 64% dos participantes pediátricos (n=20, idade de 4 a 17 anos) e 36% adultos (n=11). Injeções subretinianas bilaterais de Voretigeno Neparvoveque foram administradas sequencialmente em dois procedimentos cirúrgicos separados com um intervalo de 6 a 18 dias.
A eficácia de Voretigeno Neparvoveque foi estabelecida com base na mudança de pontuação do teste de mobilidade de luminância múltipla (MLMT) desde o início até o ano 1.
O MLMT foi projetado para medir mudanças na visão funcional, especificamente a capacidade de um participante de percorrer um percurso com precisão e em um ritmo razoável em diferentes níveis de iluminação ambiental.
O MLMT foi avaliado usando os dois olhos (visão binocular) e cada olho separadamente em um ou mais dos sete níveis de iluminação, variando de 400 lux (correspondente a um escritório muito iluminado) a 1 lux (correspondendo a uma noite de verão sem lua). Cada nível de luz foi atribuído um código de pontuação que varia de 0 a 6. Uma maior pontuação indicava que o participante conseguiu passar o MLMT em um nível de luz mais baixo. O MLMT de cada participante foi filmado e avaliado por avaliadores independentes usando uma combinação definida de pontuações de velocidade e exatidão. A pontuação do MLMT foi determinada pelo menor nível de luz em que o participante foi capaz de passar pelo MLMT. A mudança da pontuação do MLMT foi definida como a diferença entre a pontuação do início e a pontuação do ano 1. Uma mudança positiva na pontuação do MLMT, do início até a visita do ano 1, indicou que o participante era capaz de concluir o MLMT em um nível de luz mais baixo.
Três desfechos secundários também foram testados: teste de limiar de sensibilidade à luz de campo total (FST) usando luz branca; a mudança na pontuação do MLMT para o primeiro olho atribuído; e teste de acuidade visual (AV).
A Tabela 2-1 resume a variação média da classificação do MLMT desde o início até o ano 1 no grupo de tratamento de Voretigeno Neparvoveque em comparação com o grupo de controle.
Tabela 2-1 Mudanças na pontuação do MLMT: Ano 1, comparado ao início (população ITT: n=21 Intervenção, n=10 Controle)
| Mudança na pontuação do MLMT | Diferença (IC 95%) Controle de Intervenção | Valor de p |
| Usando visão binocular | 1.6 (0.72, 2.41) | 0.001 |
| Usando somente o primeiro olho atribuído | 1.7 (0.89, 2.52) | 0.001 |
| Usando somente o segundo olho atribuído | 2.0 (1.14, 2.85) | < 0.001 |
A pontuação de mudança do MLMT monocular melhorou significativamente no grupo de tratamento e foi semelhante aos resultados do MLMT binocular (consulte Tabela 2-1).
A Tabela 2-2 mostra o número e a porcentagem de pacientes com diferentes magnitudes de mudança na pontuação do MLMT usando os dois olhos no ano 1. Onze dos 21 (52%) participantes do grupo de tratamento de Voretigeno Neparvoveque tiveram uma mudança na pontuação do MLMT de dois ou mais, enquanto um dos dez (10%) participantes do grupo de controle teve uma mudança na pontuação do MLMT de dois.
Tabela 2-2 Magnitude da mudança da pontuação do MLMT usando os dois olhos no ano 1
| Mudança de pontuação | Voretigeno Neparvoveque (n=21) | Controle (n=10) |
| -1 | 0 | 3 (30%) |
| 0 | 2 (10%) | 3 (30%) |
| 1 | 8 (38%) | 3 (30%) |
| 2 | 5 (24%) | 1 (10%) |
| 3 | 5 (24%) | 0 |
| 4 | 1 (4%) | 0 |
A Figura 2-1 mostra o desempenho de MLMT de pacientes individuais usando os dois olhos no início e no ano 1.
Figura 2-1 Pontuação do MLMT usando os dois olhos no início e no ano 1 para participantes individuais
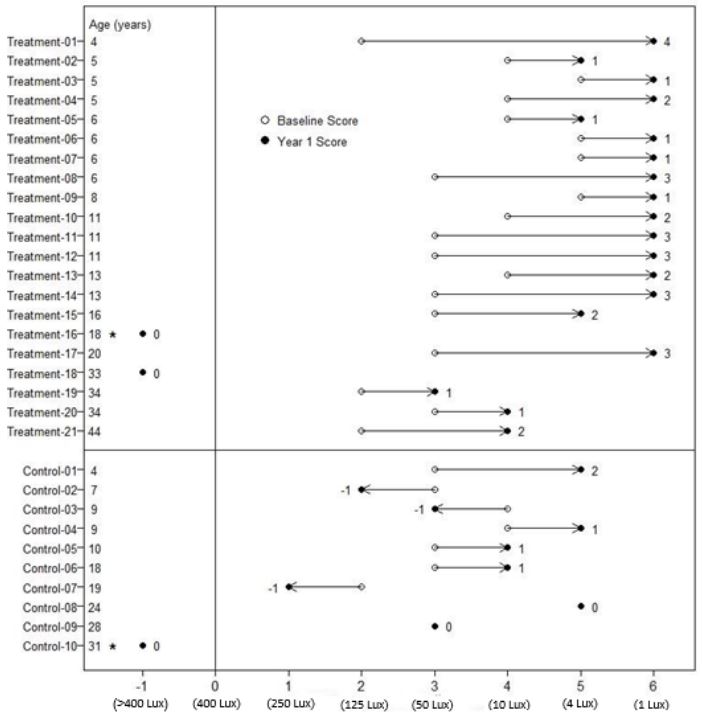
O figura 2-1 relaciona os participantes, considerando as diferentes idades, com os níveis de iluminação ( > 400 a 1 Lux).
Nota para Figura 2-1: *participantes que foram retirados ou descontinuados. Os círculos abertos são as pontuações do início. Os círculos fechados são as pontuações do ano 1. Os números ao lado do círculo sólido representam a mudança de pontuação no ano 1. As linhas horizontais com setas representam a magnitude da mudança de pontuação e sua direção. Setas apontando para a direita representam melhora. A seção superior mostra os resultados dos 21 participantes do grupo de tratamento. A seção inferior mostra os resultados dos 10 participantes no grupo de controle. Os participantes de cada grupo são cronologicamente organizados por idade, com o participante mais jovem no topo e o participante mais velho na parte inferior.
A Figura 2-2 mostra o efeito do medicamento ao longo do período de três anos no grupo de tratamento com voretigeno neparvoveque, bem como o efeito no grupo de controle após o cruzamento para receber injeção subretiniana de voretigeno neparvoveque. Diferenças significativas no desempenho do MLMT binocular foram observadas no grupo de tratamento com voretigeno neparvoveque no dia 30 e foram mantidas durante as visitas restantes de acompanhamento ao longo do período de três anos, comparado a nenhuma mudança no grupo de controle. No entanto, após o cruzamento para receber injeção subretiniana de voretigeno neparvoveque, os participantes do grupo de controle apresentaram uma resposta semelhante ao voretigeno neparvoveque comparado com os participantes do grupo de tratamento voretigeno neparvoveque.
Figura 2-2 Mudança na pontuação do MLMT usando visão binocular versus tempo antes/depois da exposição ao voretigeno neparvoveque
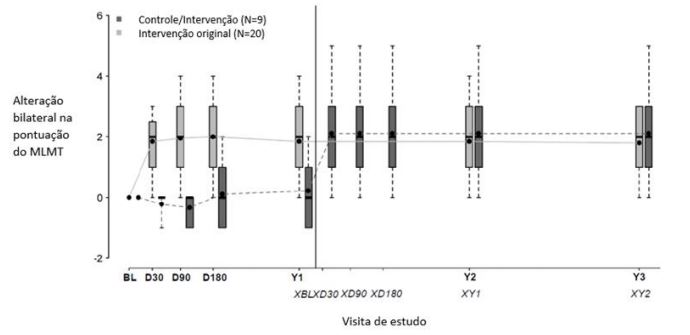
Nota para Figura 2-2: Cada caixa representa os 50% do meio da distribuição da mudança de pontuação do MLMT. Linhas pontilhadas verticais representam os 25% adicionais acima e abaixo da caixa. A barra horizontal dentro de cada caixa representa a mediana. O ponto dentro de cada caixa representa a média. A linha sólida conecta as alterações médias de pontuação do MLMT durante as visitas para o grupo de tratamento. A linha pontilhada conecta a variação média de pontuação do MLMT sobre as visitas para o grupo de controle, incluindo cinco visitas durante o primeiro ano sem receber voretigeno neparvoveque. Foi administrado voretigeno neparvoveque ao grupo de controle após 1 ano de observação.
- BL: baseline [avaliação inicial]; D30, D90, D180: 30, 90 e 180 dias após o início do estudo;
- Y1, Y2, Y3: um, dois e três anos após o início do estudo;
- XBL; XD30; XD90; XD180: avaliação inicial, 30, 90 e 180 dias após o início do estudo para o grupo de cruzamento de controle;
- XY1; XY2: um e dois anos após o início do estudo para o grupo de cruzamento de controle.
O teste de FST é uma medida global da sensibilidade da retina à luz, em que os valores de Log10 (cd.s/m2 ) indicam melhor sensibilidade quando são mais negativos. Resultados do teste de sensibilidade à luz em campo total no primeiro ano de estudo: luz branca [Log10 (cd.s/m2 )] são mostrados na Tabela 2-3 a seguir.
Tabela 2-3 Teste de sensibilidade à luz de campo total
| Teste de sensibilidade à luz de campo total - Primeiro olho atribuído (ITT) | |||
| Intervenção, N = 21 | |||
| Início | Ano 1: | Mudança | |
| N | 20 | 20 | 19 |
| Média (SE) | -1.23 (0.10) | -3.44 (0.30) | -2.21 (0.30) |
| Controle, N = 10 | |||
| N | 9 | 9 | 9 |
| Média (SE) | -1.65 (0.14) | -1.54 (0.44) | 0.12 (0.45) |
| Diferença (IC 95%) (Intervenção-Controle) -2.33 (-3.44, -1.22), p < 0.001 | |||
| Teste de sensibilidade à luz de campo total - Segundo olho atribuído (ITT) | |||
| Intervenção, N = 21 | |||
| Início | Ano 1: | Mudança | |
| N | 20 | 20 | 19 |
| Média (SE) | -1.35 (0.09) | -3.28 (0.29) | -1.93 (0.31) |
| Controle, N = 10 | |||
| N | 9 | 9 | 9 |
| Média (SE) | -1.64 (0.14) | -1.69 (0.44) | 0.04 (0.46) |
| Diferença (IC 95%) (Intervenção-Controle) -1.89 (-3.03, -0.75), p=0.002 | |||
| Teste de sensibilidade à luz de campo total - Média entre os dois olhos (ITT) Diferença (IC 95%) (Intervenção-Controle): -2.11 (-3.19, -1.04), p < 0.001 | |||
Os participantes do grupo de controle que cruzaram para receber uma injecção subretiniana de voretigeno neparvoveque no ano 1 apresentaram uma resposta semelhante ao voretigeno neparvoveque como participantes no grupo de intervenção original. Para ambos os grupos de tratamento, após a administração do vetor, o ganho no desempenho do FST foi maior que 2 unidades log, refletindo uma melhora de mais de 100 vezes na sensibilidade à luz. A melhora na sensibilidade à luz de campo total foi mantida por até 3 anos após a exposição ao voretigeno neparvoveque.
Uma análise de suporte mostrou que as relações lineares entre as pontuações do MLMT e FST neste estudo foram geralmente boas a fortes, indicando que os participantes com melhora no teste de mobilidade no ano 1 tenderam a ter resultados FST menores (ou seja, melhores) no ano 1.
Um ano após a exposição ao voretigeno neparvoveque, a mudança média em relação ao início na acuidade visual em ambos os olhos usando a escala de Holladay foi de -0,16 LogMAR para o grupo de intervenção e de 0,01 LogMAR para o grupo de controle não tratado. Isso refletiu uma melhora média de 8 letras ETDRS para os participantes de intervenção, comparado com uma perda média de 0,5 letras para os participantes de controle. Essa diferença entre os grupos não foi estatisticamente significativa.
Em uma análise post hoc de apoio usando a escala de Lange para pontuação fora do quadro, o grupo de intervenção mostrou uma melhora de 9,0 letras versus uma melhora de 1,5 letras no grupo de controle, média de ambos os olhos (diferença de 7,5 letras). Essa diferença entre os grupos foi estatisticamente significativa.
Dados de segurança não clínicos
A administração subretiniana simultânea e bilateral de voretigeno neparvoveque foi bem tolerada em níveis de dose até 8,25 x 1010 gv por olho em cães com uma mutação RPE-65 de ocorrência natural e 7,5 x 1011 gv (5 vezes superior à dose humana recomendada) por olho em primatas não humanos (NHPs) com olhos com visão normal. Em ambos os modelos animais, administrações sequenciais subretinianas bilaterais, onde o olho contralateral foi injetado após o primeiro olho, foram bem toleradas no nível de dose humana recomendada de 1,5 x 1011 gv por olho. Além disso, os cães com a mutação RPE-65 apresentaram melhor comportamento visual e respostas pupilares.
A histopatologia ocular de olhos de cão e de primatas não humanos expostos ao voretigeno neparvoveque mostrou apenas mudanças leves, que foram principalmente relacionadas com a cicatrização de lesão cirúrgica. Em um estudo toxicológico anterior, um vetor AAV2 semelhante administrado subretinianamente em cães em uma dose de 10 vezes a dose recomendada resultou em toxicidade focal da retina e infiltrados celulares inflamatórios histologicamente em regiões expostas ao vetor. Outros achados de estudos não clínicos de voretigeno neparvoveque incluíram células inflamatórias ocasionais e isoladas na retina, sem degeneração aparente da retina. Após a administração de um único vetor, os cães desenvolveram anticorpos contra o capsídeo do vetor AAV2 que estavam ausentes em primatas não humanos naïve.
Carcinogenicidade e mutagenicidade
Não foram realizados estudos em animais para avaliar os efeitos da voretigeno neparvoveque na carcinogenicidade ou mutagenicidade.
Referências bibliográficas
- LTW888 - voretigeno neparvoveque. 7010592_CG_A-23P-967. Quality Overall Summary – Drug product. Novartis. 29-Mar-2019.
- Luxturna (voretigeno neparvoveque). Pharmacy manual for the dose preparation of Voretigeno Neparvoveque. January 2019.
- Luxturna (voretigeno neparvoveque). LTW888A1 – 2.5 Clinical Overview in Biallelic RPE65 mutation-associated retinal dystrophy. Novartis. 29-Mar-2019.
- Luxturna (voretigeno neparvoveque). Surgical manual for the administration of Voretigeno Neparvoveque. January 2019.
- Luxturna (voretigeno neparvoveque). LTW888A1 – 2.7.4 Summary of Clinical Safety in confirmed biallelic RPE65 mutation-associated retinal dystrophy. Novartis. 26-Mar-2019.
- LTW888 (voretigeno neparvoveque). 2.4 Nonclinical Overview. Novartis. 24-Jan-2019.
- LTW888 Voretigeno neparvoveque (AAV2-hRPE65v2). 2.7.2 Summary of Clinical Pharmacology Studies. Novartis. 14-Feb-2019.
- LTW888 (voretigeno neparvoveque). 2.7.3 Summary of Clinical Efficacy in Biallelic RPE65 mutationassociated retinal dystrophy. Novartis. 27-Mar-2019.
Características Farmacológicas
Grupo farmacoterapêutico: Outros oftalmológicos - voretigeno neparvoveque.
Código ATC: S01XA27.
Mecanismo de ação
O Voretigeno Neparvoveque foi concebido para fornecer uma cópia normal do gene que codifica a proteína de 65 kDa (RPE65) do epitélio pigmentado retiniano humano para as células da retina em pessoas com níveis reduzidos ou ausentes de RPE65 biologicamente ativo. O RPE65 é produzido nas células do epitélio pigmentado retiniano (EPR) e converte todo o trans-retinol em 11-cis-retinol, que subsequentemente forma o cromóforo, 11 cis-retinal, durante o ciclo visual (retinoide). O ciclo visual é crítico na fototransdução, que se refere à conversão biológica de um fóton de luz em um sinal elétrico na retina. Mutações no gene RPE65 levam a níveis reduzidos ou ausentes da atividade do isômero hidrolase do RPE65, bloqueando o ciclo visual, resultando em comprometimento da visão e, por fim, cegueira completa.
Farmacodinâmica
A injeção de Voretigeno Neparvoveque no espaço subretiniano resulta na transdução de algumas células do epitélio pigmentado retiniano com um cDNA que codifica a proteína RPE65 humana normal, fornecendo assim o potencial para restaurar o ciclo visual.
Farmacocinética
Biodistribuição (dentro do corpo) e Eliminação de Vetor (excreção/secreção)
Os níveis de DNA de vetor de Voretigeno Neparvoveque em vários tecidos e secreções foram determinados usando um ensaio quantitativo de reação em cadeia da polimerase (qPCR).
Dados não clínicos
A biodistribuição de voretigeno neparvoveque foi avaliada aos três meses após a administração subretiniana em primatas não humanos. Os níveis mais altos de sequências de DNA de vetor foram detectados em fluidos intraoculares (líquido de câmara anterior e vítreo) de olhos injetados com vetor. Níveis baixos de sequências de DNA de vetor foram detectados no nervo óptico do olho injetado pelo vetor, quiasma óptico, baço e fígado, e esporadicamente nos linfomodos. Sequências de DNA de vetor não foram detectadas nas gônadas.
Dados clínicos
A eliminação e a biodistribuição do vetor de Voretigeno Neparvoveque foram investigados em um estudo medindo o DNA de Voretigeno Neparvoveque em lágrimas de ambos os olhos, no soro e sangue total de participantes do Estudo 301. Em resumo, o vetor de Voretigeno Neparvoveque foi eliminado transitoriamente e em níveis baixos em lágrimas do olho injetado em 45% dos participantes no Estudo 301 e ocasionalmente (7%) do olho não injetado até o Dia 3 após a injeção.
Em 29 participantes que receberam administrações bilaterais, o DNA de vetor de Voretigeno Neparvoveque estava presente em amostras de lágrimas de 13 participantes (45%). Níveis máximos de DNA de vetor foram detectados nas amostras de lágrimas no dia 1 após a injeção, após o dia 1 nenhum vetor de DNA foi detectado na maioria dos participantes (8 de 13). Três participantes (10%) tinham DNA de vetor em amostras de lágrimas até o dia 3 após a injeção, e dois participantes (7%) tinham DNA de vetor em amostras de lágrima por cerca de duas semanas após a injeção. Em outros dois participantes (7%), o DNA de vetor foi detectado em amostras de lágrimas do olho não injetado (ou previamente injetado) até o dia 3 após a injeção. DNA de vetor foi detectado no soro em 3/29 (10%) participantes, incluindo dois com DNA de vetor em amostras de lágrima até o dia 3 após cada injeção.

 Revisado por Isabelle Baião de Mello Neto (CRF-MG 24309)
Revisado por Isabelle Baião de Mello Neto (CRF-MG 24309)