Qual a ação da substância do Empaveli?
Resultados de Eficácia
A eficácia e a segurança de pegcetacoplana em pacientes com HPN foi avaliada em dois estudos de Fase 3 abertos e controlados randomicamente: Estudo APL2-302 (NCT03500549) e Estudo APL2-308 (NCT04085601). Todos os pacientes que completaram os estudos foram elegíveis a se inscreverem em um estudo separado de extensão a longo prazo.
Em ambos os estudos, os pacientes foram vacinados contra Streptococcus pneumoniae, Neisseria meningitidis tipos A, C, W, Y, e B, e Haemophilus influenzae tipo B (Hib), ou dentro de 2 anos antes do Dia 1 ou dentro de 2 semanas após iniciar o tratamento com pegcetacoplana. Os pacientes vacinados após o 1º dia receberam tratamento profilático com antibióticos apropriados até 2 semanas após a vacinação. Além disso, a antibioticoterapia profilática foi administrada a critério do investigador de acordo com as diretrizes de tratamento local para pacientes com HPN que estão recebendo tratamento com um inibidor de complemento.
A dose de pegcetacoplana foi de 1.080 mg duas vezes por semana em pacientes randomizados para o grupo pegcetacoplana de cada estudo. Se necessário, a dose de pegcetacoplana podia ser ajustada para 1.080 mg a cada 3 dias. O pegcetacoplana foi administrado como uma infusão subcutânea; o tempo de infusão foi de aproximadamente 20 a 40 minutos.
Estudo em pacientes adultos com PNH tratados com inibidor de complemento - Estudo APL2-302
O Estudo APL2-302 foi um estudo Fase 3 de 16 semanas, randomizado, aberto, controlado por comparador ativo seguido por um período aberto (OLP) de 32 semanas. Este estudo envolveu pacientes com HPN que haviam sido tratados com uma dose estável de eculizumabe por pelo menos 3 meses anteriores e com níveis de Hb ≤ 10,5 g/dL.
Os pacientes elegíveis entraram em um período de run-in de 4 semanas durante o qual receberam 1.080 mg de pegcetacoplana por via subcutânea duas vezes por semana, além da dose atual de eculizumabe. Os pacientes foram então randomizados em uma proporção de 1:1 para receber 1.080 mg de pegcetacoplana duas vezes por semana ou sua dose atual de eculizumabe durante o período controlado randomizado (RCP) de 16 semanas. Se necessário, a dose de pegcetacoplana pode ser ajustada para 1080 mg a cada 3 dias.
A randomização foi estratificada com base no número de transfusões de concentrado de hemácias (PRBC) nos 12 meses anteriores ao Dia -28 (<4; ≥4) e contagem de plaquetas na triagem (<100.000/mm3 ; ≥100.000/mm3). Após a conclusão do RCP, os pacientes entraram em um período aberto de 32 semanas e receberam monoterapia com pegcetacoplana. Os pacientes inicialmente randomizados para eculizumabe durante o RCP entraram em um período de 4 semanas antes de migrar para a monoterapia de pegcetacoplana. Todos os pacientes que completaram o período de 48 semanas foram elegíveis para se inscrever em um estudo de extensão de longo prazo separado.
Os desfechos primários e secundários de eficácia foram avaliados na Semana 16. O desfecho primário de eficácia foi a mudança no nível de hemoglobina da linha de base até a Semana 16 (durante o RCP). A linha de base foi definida como a média das medidas registradas antes de tomar a primeira dose de pegcetacoplana. Os principais desfechos secundários de eficácia foram a prevenção de transfusão, definida como a proporção de pacientes que não necessitaram de transfusão durante o RCP, e a mudança na contagem absoluta de reticulócitos (CAR), nível de LDH (lactato desidrogenase) e pontuação na escala de fadiga FACIT da linha de base até a Semana 16.
Um total de 80 pacientes foram randomizados para receber tratamento, 41 para pegcetacoplana e 39 para eculizumabe nos regimes de dosagem recomendada por 16 semanas. As características demográficas e da doença de base foram geralmente bem equilibradas entre os grupos de tratamento (ver Tabela 1). Um total de 38 pacientes do grupo tratado com pegcetacoplana e 39 pacientes do grupo eculizumabe completaram o RCP de 16 semanas e continuaram no OLP de 32 semanas. Conforme o protocolo, 15 pacientes tiveram sua dose ajustada para 1080 mg a cada três dias. Doze pacientes foram avaliados para benefício e 8 dos 12 pacientes demonstraram benefício com o ajuste de dose.
Tabela 1: Demografia e Características da Linha de Base dos Pacientes no Estudo APL2-302
| Parâmetro | Estatística | Pegcetacoplana (N=41) | Eculizumabe (N=39) |
| Idade (anos) | Média (DP) | 50,2 (16,3) | 47,3 (15,8) |
| Nível de dose de eculizumabe na linha de base | |||
| A cada 2 semanas 900 mg IV | n (%) | 26 (63,4) | 29 (74,4) |
| A cada 11 dias 900 mg IV | n (%) | 1 (2,4) | 1 (2,6) |
| A cada 2 semanas 1200 mg IV | n (%) | 12 (29,3) | 9 (23,1) |
| A cada 2 semanas 1500 mg IV | n (%) | 2 (4,9) | 0 |
| Sexo | |||
| Feminino | n (%) | 27 (65,9) | 22 (56,4) |
| Tempo desde o diagnóstico de HPN (anos) até o Dia 28 | Média (DP) | 8.7 (7,4) | 11.4 (9,7) |
| Nível de hemoglobina (g/dL) | Média (DP) | 8.7 (1,1) | 8,7 (0,9) |
| Contagem de reticulócitos absolutos (109 células/L) | Média (DP) | 218 (75,0) | 216 (69,1) |
| Nível de LDH (U/L) | Média (DP) | 257.5 (97,6) | 308.6 (284,8) |
| Pontuação total de fadiga FACIT | Média (DP) | 32,2 (11,4) | 31,6 (12,5) |
| Número de transfusões nos últimos 12 meses anteriores ao Dia -28 | Média (DP) | 6.1 (7,3) | 6.9 (7,7) |
| <4 | n (%) | 20 (48,8) | 16 (41,0) |
| ≥4 | n (%) | 21 (51,2) | 23 (59,0) |
| Contagem de plaquetas na triagem (109 /L) | Média (DP) | 167 (98,3) | 147 (68.8) |
| <100,000/mm3 | 12 (29,3) | 9 (23,1) | |
| ≥100,000/mm3 | 29 (70,7) | 30 (76,9) | |
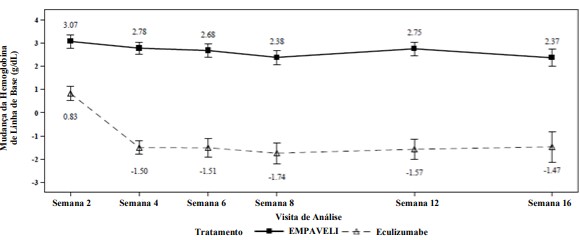
A pegcetacoplana foi superior ao eculizumabe para o desfecho primário de mudança no nível de hemoglobina de linha de base (p <0,0001). A alteração média ajustada da linha de base no nível de hemoglobina foi de 2,4 g/dL no grupo tratado com pegcetacoplana versus -1,5 g/dL no grupo eculizumabe, demonstrando um aumento médio ajustado de 3,8 g/dL com pegcetacoplana em comparação com eculizumabe na Semana 16 (Figura 1). As diferenças de tratamento entre os grupos pegcetacoplana e eculizumabe foram evidentes já na segunda semana e persistiram durante as 16 semanas de RCP.
Figura 1: Mudança Média Ajustada (± EP) da Linha de Base até a Semana 16 na Hemoglobina (g/dL) no Estudo APL2-302
A não-inferioridade foi demonstrada nos principais desfechos secundários de prevenção de transfusão e CAR. A prevenção de transfusão foi alcançada em 85% dos pacientes do grupo tratado com pegcetacoplana, em comparação com 15% no grupo eculizumabe. No grupo tratado com pegcetacoplana, a mudança média ajustada da linha de base na CAR foi 136×109 /L contra 28×109 /L no grupo eculizumabe, demonstrando uma diminuição média ajustada de 164×109 /L em comparação com o eculizumabe.
A não inferioridade não foi alcançada na mudança no LDH de linha de base; entretanto, a mudança média ajustada da linha de base no LDH foi de 15 U/L no grupo tratado com pegcetacoplana e 10 U/L no grupo eculizumabe, demonstrando um decréscimo médio ajustado de 5 U/L em comparação com o eculizumabe.
A mudança média ajustada da linha de base na pontuação de fadiga FACIT foi de 9,2 pontos no grupo tratado com pegcetacoplana contra 2,7 pontos no grupo eculizumabe, demonstrando um aumento médio ajustado de 11,9 pontos em comparação com o eculizumabe. Devido a testes hierárquicos, a mudança da linha de base para este parâmetro não foi testada formalmente.
As médias ajustadas, diferenças de tratamento, intervalos de confiança (ICs) e análises estatísticas realizadas para os principais desfechos secundários são mostrados na Figura 2.
Figura 2: Análise dos Principais Desfechos Secundários
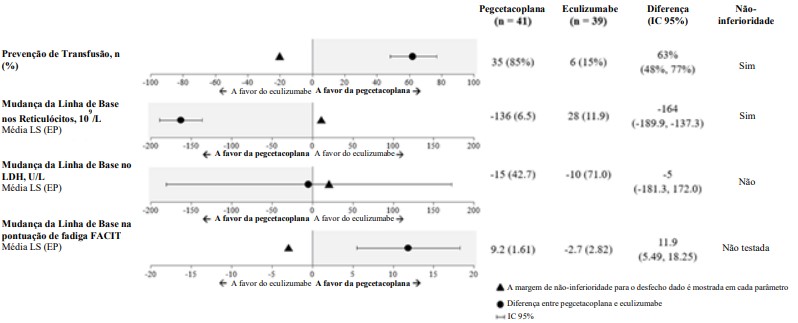
Os resultados foram consistentes em todas as análises de apoio dos desfechos primários e secundários principais, incluindo todos os dados observados com dados pós-transfusão incluídos.
Em pacientes tratados com pegcetacoplana, as análises de eficácia primária e secundária principal não mostraram diferenças notáveis com base no sexo, raça ou idade.
A normalização da hemoglobina foi alcançada em 34% dos pacientes no grupo pegcetacoplana contra 0% no grupo eculizumabe na Semana 16. A normalização da CAR foi alcançada em 78% dos pacientes do grupo tratado com pegcetacoplana contra 3% no grupo eculizumabe. A normalização do LDH foi alcançada em 71% dos pacientes do grupo tratado com pegcetacoplana contra 15% do grupo eculizumabe.
Todos os 77 pacientes que concluíram o RCP entraram no OLP de 32 semanas, durante o qual todos os pacientes receberam pegcetacoplana, resultando em uma exposição total de até 48 semanas. Os resultados de eficácia na Semana 48 foram geralmente consistentes com os da Semana 16.
Estudo em pacientes adultos com PNH não tratados com inibidor de complemento - Estudo APL2-308
O estudo APL2-308 foi um estudo randomizado, aberto e controlado por padrão de tratamento (Braço controle) que inscreveu pacientes com HPN que não tinham sido tratados com nenhum inibidor de complemento nos 3 meses anteriores à inscrição e com níveis de Hb inferiores ao limite inferior do normal (LIN). Os pacientes elegíveis foram randomizados em uma proporção de 2:1 para receber pegcetacoplana ou cuidados de suporte excluindo inibidores de complemento (por exemplo: transfusões, costicoesteroides, suplementos como ferro, folato ou vitamina B12), através da duração do período de tratamento de 26 semanas.
A randomização foi estratificada com base no número de transfusões de glóbulos vermelhos (PRBC) nos 12 meses anteriores ao Dia 28 (<4; ≥4). Em qualquer ponto durante o estudo, um paciente designado para o grupo de tratamento SoC que tinha níveis de Hb ≥2 g/dL abaixo da linha de base ou apresentado um evento tromboembólico associado à HPN foi, por protocolo, capaz de fazer a transição para pegcetacoplana para o restante do estudo.
Um total de 53 pacientes foram randomizados, 35 para pegcetacoplana e 18 pacientes para Braço controle. A demografia e as características da doença de base foram geralmente bem equilibradas entre os grupos de tratamento (ver Tabela 2). Onze dos 18 pacientes randomizados para Braço controle transitaram para pegcetacoplana porque seu nível de Hb diminuiu em ≥2 g/dL abaixo da linha de base. Por protocolo, três pacientes tiveram sua dose ajustada para 1.080 mg a cada três dias.
Tabela 2: Dados Demografia e Características da Linha de Base do Paciente no Estudo APL2 308
| Parâmetro | Estatística | Pegcetacoplana (N=35) | Braço controlea (N=18) |
| Idade (anos) | Média (DP) | 42,2 (12,7) | 49.1 (15.6) |
| Sexo | |||
| Feminino | n (%) | 16 (45,7) | 8 (44.4) |
| Raça | |||
| Índio americano ou nativo do Alasca | n (%) | 9 (25,7) | 2 (11.1) |
| Asiático | n (%) | 23 (65,7) | 16 (88,9) |
| Negro ou afro-americano | n (%) | 2 (5,7) | 0 |
| Outro | n (%) | 1 (2,9) | 0 |
| Etnicidade | |||
| Hispânico ou Latino | n (%) | 12 (34,3) | 2 (11,1) |
| Não Hispânico ou Latino | n (%) | 23 (65,7) | 16 (88,9) |
| Tempo desde o diagnóstico de HPN (anos) até a Visita 2 (Semana 0) | Média (DP) | 5,7 (5,9) | 5,5 (5,1) |
| Nível de hemoglobina (g/dL) | Média (DP) | 9,4 (1,4) | 8,7 (0,8) |
| Contagem absoluta de reticulócito (109 células/L) | Média (DP) | 230,2 (81,0) | 180,3 (109,1) |
| Nível de LDH (U/L) | Média (DP) | 2151.0 (909.4) | 1945,9 (1003,7) |
| Pontuação total de fadiga FACIT | Média (DP) | 36,3 (10,7) | 37,1 (9,3) |
| Número de transfusões nos últimos 12 meses antes do Dia 28 | Média (DP) | 3,9 (4,4) | 5,1 (5,0) |
| <4 | n (%) | 21 (60,0) | 8 (44,4) |
| ≥4 | n (%) | 14 (40,0) | 10 (55,6) |
| Contagem plaquetária (células × 109 /L) | Média (DP) | 191,4 (118,7) | 125,5 (51,1) |
a Braço Controle = Cuidados de suporte (excluindo inibidores de complemento).
Os pontos finais de eficácia primários e secundários foram avaliados na Semana 26. Os dois pontos finais de eficácia primários co-principais foram a estabilização de Hb, definida como a prevenção de uma diminuição de >1 g/dL na concentração de Hb desde o início, na ausência de transfusão, e a mudança na concentração de LDH desde o início.
Pegcetacoplana foi superior ao SoC para o primeiro ponto final co-primário de estabilização de Hb até a Semana 26 (p<0.0001). No grupo tratado com pegcetacoplana, 30 de 35 pacientes (85,7%) alcançaram a estabilização de Hb versus 0 pacientes no grupo SoC. A diferença ajustada entre pegcetacoplana e SoC foi de 73,1% (IC 95%, 57,2% a 89,0%).
Pegcetacoplana também foi superior ao SoC para o segundo ponto final co-primário de mudança desde o início na concentração de LDH na Semana 26 (p<0.0001). As mudanças médias (LS) mínimas quadradas (SE) desde o início em LDH foram de -1870 U/L no grupo tratado com pegcetacoplana e versus -400 U/L no grupo SoC. A diferença entre pegcetacoplana e SoC foi de -1470 (IC 95%, -2113 a -827). As diferenças de tratamento entre os grupos pegcetacoplana e SoC foram evidentes na Semana 2 e foram mantidas até a Semana 26 (Figura 3). As concentrações de LDH no grupo SoC permaneceram elevadas.
Figura 3 Média (±SE) de Concentração de LDH (U/L) ao Longo do Tempo por Grupo de Tratamento no Estudo APL2-308
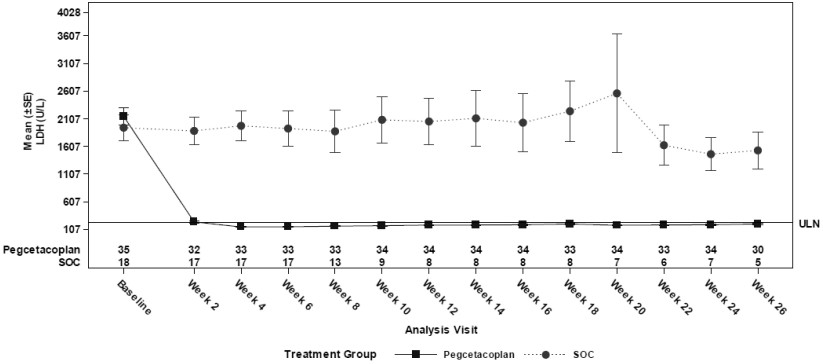
Para os pontos finais secundários de eficácia de mudança desde o início em ARC, mudança desde o início em Hb e evitamento de transfusão, foi demonstrada superioridade para pegcetacoplana versus SoC.
No grupo tratado com pegcetacoplana, a mudança média desde o início em ARC foi de 123 × 109/L versus 19 × 109/L no SoC, demonstrando uma diminuição média ajustada de 104 × 109/L comparada ao SoC.
No grupo tratado com pegcetacoplana, a mudança média desde o início em Hb foi de 2,94 g/dL versus 0,27 g/dL no SoC, demonstrando uma diferença média ajustada de 2,67 g/dL comparada ao SoC.
O evitamento de transfusão foi alcançado em 91% dos pacientes no grupo tratado com pegcetacoplana, em comparação com 6% no grupo SoC.
Não foi demonstrada superioridade para a mudança desde o início no escore de fadiga FACIT, no entanto, a mudança média ajustada desde o início no escore de fadiga FACIT foi de 7,8 pontos no grupo tratado com pegcetacoplana versus 3,3 pontos no grupo SoC, demonstrando um aumento médio ajustado de 4,5 pontos comparado ao SoC.
As médias ajustadas, diferença de tratamento, intervalos de confiança e análises estatísticas realizadas para os pontos finais secundários selecionados são mostrados na Tabela 3.
Os resultados de eficácia são apresentados na Tabela 3 abaixo.
Tabela 3: Resultados de eficácia durante o estudo de 26 semanas no Estudo APL2-308
| Pegcetacoplana (N=35) | Braço controlea (N=18) | Diferença (IC de 95%) valor p | |
| Alteração desde o valor basal em ARCb | |||
| (LS† CFB média, EP‡) | -123 (9,2) | -19 (25,2) | 103 (158,9, 48,7) p = 0,0002 |
| Alteração desde o valor basal em Hbb | |||
| (LS† CFB média, EP‡) | 2,9 (0,38) | 0,3 (0,76) | 2,7 (0,99, 4,35) p = 0,0019 |
| Prevenção de transfusão§ | |||
| (n, %) | 32 (91%) | 1 (6%) | 72% (56%, 89%) p<0,0001* |
| Alteração desde o valor basal em pontuação na escala de fadiga FACIT | |||
| (LS† CFB média, EP‡) | 7.78 (1.21) | 3.26 (2.11) | 4.51 (-0.21 to 9.24) p=0.061 |
a = cuidados de suporte (excluindo inibidores de complemento).
b Os valores ausentes pós-basais (incluindo os valores após o cruzamento do braço controle) são calculados usando um método de imputação múltipla. Dados coletados após o cruzamento do braço controle são excluídos nas análises.
§ Os paciente que mudaram do grupo do braço controle para o grupo pegcetacoplana, se retiraram do estudo ou foram considerados perda de acompanhamento são considerados como insucesso em atender aos critérios.
*O valor p é obtido pelo teste estratificado de Cochran-Mantel-Haenszel.
† LS = Quadrado mínimo.
‡ EP = Erro padrão.
Referência Bibliográfica
Hillmen P, Szer J, Weitz I, et al. Pegcetacoplan versus eculizumab in paroxysmal nocturnal hemoglobinuria. N Engl J Med 2021;384:1028-37.
Peffault de Latour R, Szer J, Weitz IC, et al. Pegcetacoplan versus eculizumab in patients with paroxysmal nocturnal haemoglobinuria (PEGASUS): 48-week follow-up of a randomised, open-label, phase 3, active-comparator, controlled trial. Lancet Haematol 2022;9:e648-59. Para o Estudo APL2-308: https://www.clinicaltrialsregister.eu/ctr-search/trial/2018-004220-11/results.
Características Farmacológicas
Propriedades farmacodinâmicas
Grupo farmacoterapêutico: imunossupressores seletivos, código ATC: LO4AA54.
A pegcetacoplana é uma molécula simétrica composta por dois pentadecapeptídeos idênticos ligados covalentemente às extremidades de uma molécula linear de polietilenoglicol (PEG) de 40 kDa. As porções peptídicas ligam-se ao complemento C3 e exercem uma ampla inibição da cascata do complemento. A fração PEG de 40 kDa confere solubilidade melhorada e maior tempo de residência no corpo após a administração do medicamento.
Mecanismo de ação
A pegcetacoplana se liga à proteína C3 do complemento e seu fragmento de ativação C3b, regulando assim a clivagem de C3 e a geração de efetores a jusante da ativação do complemento. Na HPN, a hemólise extravascular (EVH) é facilitada pela opsonização de C3b, enquanto a hemólise intravascular (IVH) é mediada pelo complexo de ataque à membrana (MAC) a jusante. A pegcetacoplana exerce uma ampla regulação da cascata do complemento atuando proximalmente tanto na formação C3b quanto na formação MAC, controlando assim os mecanismos que levam ao EVH e IVH. Estas funções da pegcetacoplana estão subjacentes à redução sustentada observada na atividade hemolítica mediada do complemento em pacientes com HPN.
Efeitos farmacodinâmicos
No estudo APL2-302, a concentração média de C3 aumentou de 0,94 g/L na linha de base para 3,83 g/L na Semana 16 no grupo pegcetacoplana e foi sustentado até a Semana 48. No estudo APL2 308, a concentração média de C3 aumentou de 0,95 g/L na linha de base para 3,56 g/L na Semana 26.
No estudo APL2-302, a porcentagem de eritrócitos HPN Tipo II + III aumentou de 66,80% na linha de base para 93,85 % na Semana 16 e foi mantida até a Semana 48. No Estudo APL2 308, a porcentagem média de eritrócitos HPN Tipo II + III aumentou de 42,4% na linha de base para 90,0% na Semana 26.
No estudo APL2-302, a porcentagem média de eritrócitos HPN Tipo II + III com deposição de C3 foi reduzido de 17,73% na linha de base para 0,20% na Semana 16 e sustentado até a Semana 48. No Estudo APL2-308, a porcentagem média de eritrócitos HPN Tipo II + III com deposição de C3 diminuiu de 2,85% na linha de base para 0,09% na Semana 26.
O tratamento com pegcetacoplana de pacientes com HPN resultou na melhoria do nível de hemoglobina (Hb) e na redução da contagem absoluta de reticulócitos (CAR) e LDH.
Eletrofisiologia Cardíaca
Não foram realizados estudos específicos para determinar o potencial da pegcetacoplana para retardar a repolarização cardíaca. A pegcetacoplana é uma estrutura peptídica PEGuilada e não apresentou nenhuma inibição no ensaio de canal iônico do gene humano éter-a-go-go (hERG). A análise da concentração-QTc confirmou nenhum efeito sobre a repolarização cardíaca (intervalo QT corrigido para a frequência cardíaca).
Propriedades farmacocinéticas
Absorção
Pegcetacoplana é administrado por infusão subcutânea e absorvido gradualmente na circulação sistêmica com um Tmax de pegcetacoplana mediano entre 108 e 144 horas (4,5 a 6,0 dias) após uma dose única subcutânea em voluntários saudáveis. As concentrações séricas no estado de equilíbrio após a administração de 1.080 mg duas vezes por semana em pacientes com HPN foram alcançadas aproximadamente 4 a 6 semanas após a primeira dose e as concentrações terapêuticas da pegcetacoplana foram mantidas até a Semana 48. A exposição da pegcetacoplana aumenta de forma proporcional de 45 a 1.440 mg.
Distribuição
A média (C%V) do volume central de distribuição da pegcetacoplana é de aproximadamente 3,97 L (20%) em pacientes com HPN.
Biotransformação
Com base em sua estrutura de peptídeo PEGuilada, é esperado que a degradação da pegcetacoplana ocorra através de vias catabólicas em pequenos peptídeos, aminoácidos e PEG. Os resultados de um estudo radiomarcado em macacos cinomolgos sugerem que a principal via de eliminação da fração peptídica marcada é via excreção urinária.
Eliminação
Após múltiplas doses subcutâneas de pegcetacoplana, a depuração média estimada (CV%) (CL/F) é 0,012 L/dia (20%)e a meia-vida efetiva mediana de eliminação (t1/2) é de 8,6 dias em pacientes com HPN.
Populações especiais
Não foi identificado nenhum impacto na farmacocinética da pegcetacoplana com base na idade (18 a 81 anos) e no sexo, conforme os resultados da análise da população PK. Também foi demonstrado que a raça (Asiático vs não Asiáticos) não teve impacto; entretanto, os dados são limitados e, portanto, não são considerados conclusivos.
População idosa
Com base na análise farmacocinética da população, a depuração aparente (CL/F) em pacientes idosos e pacientes com menos de 65 anos de idade foi semelhante e nenhuma diferença aparente relacionada à idade foi observada (ver seção 8.5). O número de pacientes idosos era, no entanto, limitado.
Insuficiência renal
Em um estudo de 8 pacientes com insuficiência renal grave, definida como depuração de creatina (CrCl) inferior a 30 mL/min (com 4 pacientes com valores inferiores a 20 mL/min), a insuficiência renal não teve efeito sobre a farmacocinética da pegcetacoplana (ver seção 8.5). Não há dados clínicos disponíveis para o uso de pegcetacoplana em pacientes com doença renal em estágio terminal (DRET) que necessitam de hemodiálise.
Insuficiência hepática
Não foram realizados estudos específicos para determinar o efeito da insuficiência hepática sobre a farmacocinética da pegcetacoplana. Como a biotransformação ocorre principalmente por catabolismo, não se espera que a deficiência hepática influencie a liberação da pegcetacoplana (ver seção 8.5).
Dados de segurança pré-clínicos
Os dados toxicológicos in vitro e in vivo não revelam toxicidade de especial preocupação para os seres humanos. Os efeitos observados em animais em níveis de exposição semelhantes aos níveis de exposição clínica são descritos abaixo. Estes efeitos não foram observados em estudos clínicos.
Carcinogênese
Não foram realizados estudos de carcinogenicidade animal de longo prazo com a pegcetacoplana.
Genotoxicidade
A pegcetacoplana não foi mutagênica quando testada em uma mutação reversa bacteriana in vitro (Ames) e não foi genotóxica em um ensaio in vitro em células TK6 humanas ou em um ensaio de micronúcleo in vivo em camundongos.
Fertilidade
Os efeitos da pegcetacoplana na fertilidade não foram estudados em animais. Não houve anormalidades microscópicas nos órgãos reprodutores masculinos ou femininos em estudos de toxicidade em coelhos e macacos.
Toxicologia e/ou farmacologia animal
Em estudos toxicológicos em coelhos e macacos cynomolgus, observou-se vacuolização epitelial e infiltrados de macrófagos vacuolados em vários tecidos, incluindo os túbulos renais, após doses subcutâneas diárias de pegcetacoplana até 7 vezes a dose humana. Esses achados são atribuíveis à absorção das porções de PEG da pegcetacoplana. A degeneração renal foi observada microscopicamente em coelhos em exposições (Cmax e AUC) inferiores às da dose humana e em macacos em exposições aproximadamente 2,7 vezes superiores às da dose humana. O significado clínico desses achados é incerto.
Reprodução animal
Estudos de reprodução animal com pegcetacoplana foram realizados em macacos cynomolgus. O tratamento com pegcetacoplana de macacas cynomolgus grávidas com uma dose subcutânea de 28 mg/kg/dia (2,9 vezes a exposição humana com base na AUC) desde o período de gestação até o parto resultou em um aumento estatisticamente significativo de abortos e natimortos em comparação com os controles. Nenhum aumento de abortos ou natimortos ocorreu com uma dose de 7 mg/kg/dia (1,3 vezes a exposição humana com base na AUC). Nenhuma toxicidade materna ou efeitos teratogênicos foram observados na prole nascida a termo. Nenhum efeito de desenvolvimento foi observado em filhotes até 6 meses após o parto. A exposição sistêmica à pegcetacoplana de menos de 1% dos níveis maternos foi detectada em fetos de macacos tratados com 28 mg/kg/dia desde o período de organogênese até o segundo trimestre.
Lactação
Foi demonstrada excreção mínima (menos de 1%, não farmacologicamente significativa) de pegcetacoplana no leite em macacas; portanto, a probabilidade de exposição clinicamente relevante do lactente através do leite materno é considerada mínima.

 Revisado por Isabelle Baião de Mello Neto (CRF-MG 24309)
Revisado por Isabelle Baião de Mello Neto (CRF-MG 24309)