Para que serve o Bevyx?
Câncer no intestino que se espalhou (colorretal metastático)
Bevacizumabe, usado com quimioterapia à base de fluoropirimidina, é indicado para pacientes com câncer colorretal que se espalhou para outras partes do corpo.
Câncer de pulmão avançado ou que voltou (não pequenas células)
Bevacizumabe, combinado com quimioterapia à base de platina, é indicado como primeiro tratamento para câncer de pulmão de não pequenas células, não escamoso, que não pode ser operado, está avançado, espalhado ou voltou.
Câncer de mama que se espalhou ou voltou localmente
Bevacizumabe, junto com paclitaxel, é indicado como primeiro tratamento para pacientes com câncer de mama que voltou localmente ou se espalhou e que não receberam quimioterapia prévia para essa condição.
Bevacizumabe, combinado com capecitabina, é indicado como primeiro tratamento para câncer de mama que voltou localmente ou se espalhou, quando outras opções de quimioterapia não são adequadas.
Pacientes que usaram tratamentos com taxanos e antraciclinas nos últimos 12 meses não devem usar Bevacizumabe com capecitabina.
Câncer de rim avançado ou que se espalhou
Bevacizumabe, junto com alfainterferona 2a, é indicado como primeiro tratamento para pacientes com câncer de células renais avançado ou que se espalhou.
Câncer de ovário, trompa ou peritônio
Bevacizumabe, combinado com carboplatina e paclitaxel, é indicado como primeiro tratamento para câncer avançado de ovário, trompa uterina ou peritoneal.
Bevacizumabe, junto com carboplatina e gencitabina, é indicado para adultos com câncer de ovário, trompa ou peritoneal que voltou pela primeira vez e responde à platina, sem tratamento prévio com Bevacizumabe ou outros medicamentos similares.
Bevacizumabe, combinado com paclitaxel, topotecana ou doxorrubicina lipossomal peguilada, é indicado para pacientes com câncer de ovário, trompa ou peritoneal que voltou e não responde à platina, que usaram até dois tratamentos prévios e sem terapia anterior com Bevacizumabe.
Câncer do colo do útero
Bevacizumabe, junto com paclitaxel e cisplatina (ou paclitaxel e topotecana para quem não pode receber platina), é indicado para câncer de colo do útero persistente, que voltou ou se espalhou.
Quando não devo usar o Bevyx?
Bevacizumabe não deve ser usado por pacientes com alergia a qualquer componente do produto, a produtos de células de ovário de hamster chinês ou a outros anticorpos similares.
Gravidez e amamentação
Risco na gravidez: Categoria C.
Não use este medicamento na gravidez sem orientação médica.
A formação de vasos sanguíneos é crucial para o desenvolvimento do bebê.
Bevacizumabe pode causar problemas na gravidez ao inibir essa formação.
Não há estudos adequados em grávidas. Bevacizumabe pode atravessar a placenta e prejudicar o feto.
Foram observadas malformações fetais em mulheres tratadas com Bevacizumabe. Portanto, não use durante a gravidez. Mulheres com possibilidade de engravidar devem usar métodos contraceptivos durante o tratamento.
Os contraceptivos devem ser usados por pelo menos seis meses após a última dose de Bevacizumabe.
Fertilidade
Estudos em animais mostraram que Bevacizumabe pode afetar a fertilidade feminina. Em mulheres jovens, houve maior ocorrência de insuficiência ovariana. Na maioria, a função ovariana voltou após parar o tratamento.
Os efeitos a longo prazo são desconhecidos.
Não use este medicamento durante a amamentação.
Não se sabe se Bevacizumabe passa para o leite materno. Pode prejudicar o bebê. Interrompa a amamentação durante o tratamento e por pelo menos seis meses após a última dose.
Como usar o Bevyx?
Preparo e administração
Dilua Bevacizumabe em solução de cloreto de sódio 0,9%. A concentração final deve ficar entre 1,4 e 16,5 mg/mL.
Despreze o que sobrar no frasco. Este medicamento não contém conservantes. Verifique visualmente partículas ou alterações de cor antes de usar.
Incompatibilidades
Não há incompatibilidade com bolsas de PVC ou poliolefina. Bevacizumabe se degrada quando diluído em dextrose (5%).
Não use Bevacizumabe com soluções de dextrose ou glicose.
Descarte
Descarte o restante não usado do frasco, pois não contém conservantes.
Descarte de medicamentos vencidos ou não usados
Não descarte no lixo comum ou esgoto. Use sistemas de coleta específicos, se disponíveis.
Manuseio
Tome cuidado ao manusear Bevacizumabe.
Não aplique como injeção direta na veia ou em bolus.
A primeira dose deve ser aplicada em 90 minutos. Se bem tolerada, a segunda pode ser em 60 minutos. Se essa for bem tolerada, as próximas podem ser em 30 minutos.
Não reduza a dose por eventos adversos. Interrompa temporariamente ou suspenda se necessário.
Não ultrapasse a velocidade de infusão recomendada.
Posologia
Câncer no intestino que se espalhou (colorretal metastático)
Primeiro tratamento
Com 5-fluorouracil/leucovorin; 5-fluorouracil/leucovorin e irinotecano ou 5-fluoracil/leucovorin e oxaliplatina: 5 mg/kg a cada 2 semanas, até a doença piorar ou toxicidade inaceitável.
Com capecitabina e oxaliplatina: 7,5 mg/kg a cada 3 semanas, até a doença piorar ou toxicidade inaceitável.
Segundo tratamento sem uso prévio de Bevacizumabe
Com 5-fluorouracil e leucovorin, seguido de 5-fluorouracil com oxaliplatina: 10 mg/kg a cada 2 semanas ou 15 mg/kg a cada 3 semanas, até a doença piorar ou toxicidade inaceitável.
Segundo tratamento com uso prévio de Bevacizumabe
Com fluoropirimidina/irinotecano ou fluoropirimidina/oxaliplatina: 5 mg/kg a cada 2 semanas ou 7,5 mg/kg a cada 3 semanas, para pacientes tratados antes com Bevacizumabe, até nova progressão ou toxicidade inaceitável.
A quimioterapia no segundo tratamento deve ser diferente da usada no primeiro.
Câncer de pulmão avançado ou que voltou
Bevacizumabe é dado com quimioterapia à base de platina por até seis ciclos, seguido de Bevacizumabe sozinho até a doença piorar.
Com quimioterapia à base de cisplatina: 7,5 mg/kg a cada três semanas.
Com quimioterapia à base de carboplatina: 15 mg/kg a cada três semanas.
Mantenha o tratamento até a doença piorar.
Câncer de mama que se espalhou ou voltou localmente
Dose recomendada: 10 mg/kg a cada duas semanas ou 15 mg/kg a cada três semanas.
Mantenha o tratamento até a doença piorar.
Câncer de rim avançado ou que se espalhou
Dose recomendada: 10 mg/kg a cada duas semanas.
Mantenha o tratamento até a doença piorar.
Câncer de ovário, trompa ou peritônio
Doses recomendadas
Primeiro tratamento
15 mg/kg a cada três semanas, com carboplatina e paclitaxel por até seis ciclos, seguido de Bevacizumabe sozinho por 15 meses ou até a doença piorar.
Doença que voltou e responde à platina
15 mg/kg a cada três semanas, com carboplatina e gencitabina por até dez ciclos, seguido de Bevacizumabe sozinho até a doença piorar.
Doença que voltou e não responde à platina
10 mg/kg a cada duas semanas com paclitaxel, topotecana ou doxorrubicina lipossomal peguilada. Ou 15 mg/kg a cada três semanas com topotecana. Continue até a doença piorar ou toxicidade inaceitável.
Câncer do colo do útero
Bevacizumabe é dado com paclitaxel e cisplatina ou paclitaxel e topotecana.
Dose recomendada: 15 mg/kg a cada três semanas.
Mantenha o tratamento até a doença piorar.
Dosagens especiais
Crianças e adolescentes
Veja "Precauções".
Problemas nos rins ou fígado
Veja "Precauções".
Idosos
Não há ajuste de dose especial.
Quais cuidados devo ter ao usar o Bevyx?
Registre o nome comercial e o lote do medicamento no prontuário do paciente para rastreabilidade.
A substituição por outro medicamento biológico requer consentimento médico.
Perfurações e fístulas no sistema digestivo
Risco aumentado de perfuração gastrointestinal e da vesícula. Suspenda definitivamente se ocorrer perfuração gastrointestinal.
Pacientes com câncer de colo do útero podem ter risco aumentado de fístula entre a vagina e o trato digestivo.
Radiação prévia aumenta o risco. Todas as pacientes com perfuração ou fístula tinham histórico de radiação.
Fístula não gastrointestinal
Risco aumentado de fístulas. Suspenda definitivamente em caso de fístula traqueoesofágica ou fístula grave. Considere suspender em outros tipos de fístula.
Sangramentos
Risco aumentado de sangramento, principalmente associado ao tumor. Suspenda definitivamente em sangramentos graves. Sangramentos graves ocorrem até cinco vezes mais com Bevacizumabe.
Monitore sinais de sangramento no sistema nervoso central. Suspenda em caso de sangramento intracraniano.
Cautela em pacientes com distúrbios de coagulação ou que usam anticoagulantes.
Infecções graves nos olhos após uso não aprovado
Casos de infecções oculares graves, incluindo cegueira, foram relatados após uso intravítreo não aprovado.
Sangramento no pulmão / tosse com sangue
Pacientes com câncer de pulmão podem ter risco de sangramento pulmonar grave. Não use em pacientes com sangramento recente.
Pressão alta
Maior incidência de pressão alta, possivelmente dependente da dose. Controle a pressão antes de iniciar. Monitore durante o tratamento.
Suspenda definitivamente se a pressão não for controlada ou em crise hipertensiva.
Síndrome da Encefalopatia Posterior Reversível (SEPR)
Raros casos relatados. Sintomas geralmente melhoram em dias. Suspenda o tratamento. Segurança ao retomar é desconhecida.
Coágulos nas artérias
Maior incidência de coágulos arteriais, incluindo AVC e infarto. Suspenda definitivamente se ocorrer.
Cautela em pacientes com histórico de coágulos, diabetes ou acima de 65 anos.
Coágulos nas veias
Risco de coágulos venosos, incluindo embolia pulmonar. Pacientes com câncer de colo do útero têm risco aumentado.
Suspenda em eventos graves. Monitore rigorosamente eventos menos graves.
Insuficiência cardíaca
Casos de insuficiência cardíaca foram relatados, variando de assintomáticos a sintomáticos.
Cautela em pacientes com doença cardiovascular significativa. Maioria tinha recebido antraciclinas ou radioterapia prévia.
Neutropenia
Maiores taxas de neutropenia grave com alguns regimes de quimioterapia combinados com Bevacizumabe.
Cicatrização
Bevacizumabe pode atrapalhar a cicatrização. Complicações graves foram relatadas.
Não inicie pelo menos 28 dias após cirurgia grande ou até a ferida cicatrizar. Suspenda antes de cirurgias eletivas.
Casos raros de fasciite necrosante. Suspenda imediatamente se ocorrer.
Proteína na urina
Maior incidência de proteína na urina. Suspenda definitivamente em caso de síndrome nefrótica.
Fertilidade
Bevacizumabe pode prejudicar a fertilidade feminina. Discuta estratégias de preservação antes de iniciar.
Idosos
Idade acima de 65 anos aumenta risco de problemas vasculares arteriais.
Crianças
Segurança e eficácia não estabelecidas. Casos de osteonecrose foram relatados.
Problemas nos rins ou fígado
Não estudado em pacientes com insuficiência renal ou hepática.
Dirigir ou operar máquinas
Nenhuma evidência de que prejudique a capacidade de dirigir ou operar máquinas.
Não há informações de que cause doping.
Quais os efeitos colaterais do Bevyx?
Experiência em estudos clínicos
Perfil de segurança baseado em aproximadamente 5.200 pacientes.
Os efeitos colaterais mais graves foram
- Perfurações gastrointestinais;
- Sangramentos, principalmente em câncer de pulmão;
- Coágulos arteriais.
Efeitos colaterais mais comuns: pressão alta, fadiga, diarreia e dor abdominal.
Tabela 21. Reações adversas comuns e muito comuns:
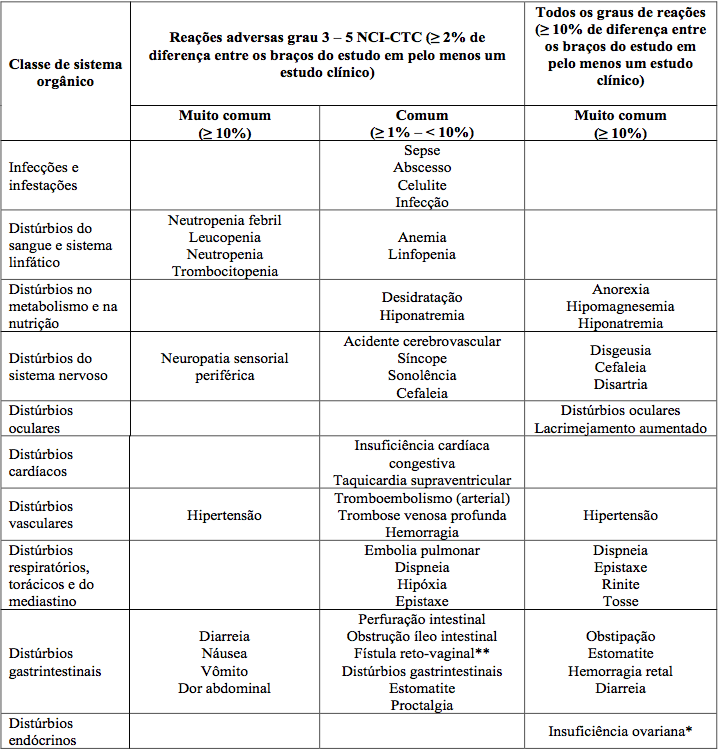
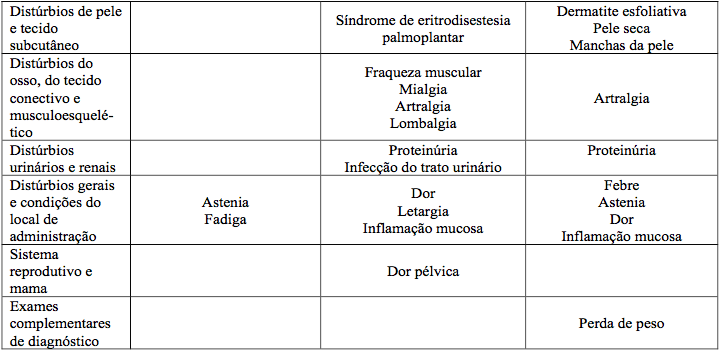
* Baseado em subestudo com 295 mulheres.
** Fístula reto-vaginal é a forma mais comum.
Reações adversas observadas
Perfuração gastrointestinal e fístula
Casos graves de perfuração gastrointestinal. Suspensão definitiva se ocorrer. Evolução fatal em um terço dos casos graves.
Fístula não gastrointestinal
Casos graves de fístula. Suspenda definitivamente em fístulas graves.
Sangramentos
Sangramentos variando de mínimos (como sangramento nasal) a graves associados ao tumor.
Pressão alta
Maior incidência de pressão alta. Geralmente controlada com medicação. Suspenda se não controlada.
Coágulos arteriais
Maior incidência de coágulos arteriais, incluindo AVC e infarto.
Coágulos nas veias
Risco de coágulos venosos, incluindo embolia pulmonar.
Insuficiência cardíaca
Casos de insuficiência cardíaca, principalmente em câncer de mama. Maioria tinha fatores de risco prévios.
Cicatrização
Pode afetar cicatrização. Não inicie até 28 dias após cirurgia grande.
Proteína na urina
Maior incidência. Suspenda definitivamente em síndrome nefrótica.
Reações à infusão
Risco de reações durante a infusão. Interrompa e trate se necessário.
Fertilidade
Pode prejudicar fertilidade feminina. Função ovariana geralmente volta após parar.
Idosos
Maior risco de coágulos arteriais e alguns efeitos colaterais.
Experiência após comercialização
Tabela 22. Reações adversas observadas após comercialização:
Classe de sistema orgânico | Reações (frequência1) |
Desordens genéticas e congênitas | Malformações fetais relatadas. |
Distúrbios do sistema nervoso | Encefalopatia hipertensiva (muito rara**). |
| Síndrome da Encefalopatia Posterior Reversível (rara***). | |
Distúrbios vasculares | Proteína na urina (frequência desconhecida). |
Distúrbios respiratórios | Perfuração do septo nasal (frequência desconhecida). |
| Pressão alta no pulmão (frequência desconhecida). | |
| Rouquidão (comum****). | |
Distúrbios gastrintestinais | Úlcera gastrintestinal (frequência desconhecida). |
Distúrbios hepatobiliares | Perfuração da vesícula (frequência desconhecida). |
Distúrbios do sistema imunológico | Reações alérgicas e à infusão (frequência desconhecida). |
Distúrbios oculares (uso não aprovado) | Infecções oculares graves (algumas com cegueira). |
| Inflamações intraoculares (algumas com cegueira). | |
| Vários métodos não validados levaram a eventos graves. | |
Eventos sistêmicos (uso não aprovado) | Maior risco de derrame hemorrágico e mortalidade global. |
Distúrbios musculoesqueléticos | Osteonecrose da mandíbula (principalmente com bisfosfonatos). |
Osteonecrose em outros locais em pacientes pediátricos6. | |
| Infecções | Fasciite necrosante (raro). |
* Se especificada, a frequência foi obtida de dados de estudos clínicos.
1 Gower et al. Adverse Event Rates Following Intravitreal Injection of Bevacizumabe or Lucentis for Treating Age-Related Macular Degeneration ARVO 2011, Poster 6644, Data on file.
2 Curtis LH, et al. Risks of mortality, myocardial infarction, bleeding, and stroke associated with therapies for age-related macular degeneration. Arch Ophthalmol. 2010;128(10):1273-1279.
3 CATT Research Group, Ranibizumab and Bevacizumabe for Neovascular Age-Related Macular Degeneration. 10.1056/NEJMoa1102673.
4 Em um caso, meningoencefalite.
5 Incluindo agrupamentos de eventos graves após administração intravenosa.
6 Osteonecrose observada em população pediátrica.
** Muito raro (<1/10.000).
*** Raro (≥1/10.000 a <1/1.000).
**** Comum (≥1/100 a <1/10).
Notifique eventos adversos pelo Sistema NOTIVISA ou Vigilância Sanitária.
Interações: o que acontece se usar Bevyx com outros remédios?
Efeito de quimioterápicos na farmacocinética
Não há interações clinicamente relevantes com quimioterápicos coadministrados.
Efeito de Bevacizumabe na farmacocinética de outros
Não altera significativamente a farmacocinética de irinotecano, capecitabina, oxaliplatina, alfainterferona 2a ou cisplatina.
Combinação com maleato de sunitinibe
Anemia hemolítica microangiopática relatada em sete de 19 pacientes. Reversível ao parar.
Radioterapia
Segurança e eficácia não estabelecidas com uso concomitante.
Como o Bevyx funciona no organismo?
Resultados da eficácia
Câncer no intestino que se espalhou
Eficácia demonstrada em estudos clínicos com diferentes regimes de quimioterapia. Bevacizumabe aumentou sobrevida global e sobrevida livre de progressão.
Câncer de pulmão avançado ou que voltou
Estudos mostraram aumento significativo de sobrevida global e sobrevida livre de progressão quando combinado com quimioterapia.
Câncer de mama que se espalhou ou voltou localmente
Aumento de sobrevida livre de progressão quando combinado com paclitaxel ou capecitabina.
Câncer de rim avançado ou que se espalhou
Aumento significativo de sobrevida livre de progressão quando combinado com alfainterferona 2a.
Câncer de ovário, trompa ou peritônio
Benefício em tratamento de primeira linha e em doença recorrente, com aumento de sobrevida livre de progressão.
Câncer do colo do útero
Aumento de sobrevida global quando combinado com quimioterapia.
Como o medicamento age
Bevacizumabe é um anticorpo monoclonal que bloqueia o fator de crescimento do endotélio vascular (VEGF), impedindo a formação de vasos sanguíneos que alimentam o tumor.
Farmacocinética
Volume central: 2,73 litros (mulheres) e 3,28 litros (homens). Meia-vida de eliminação: 18-20 dias. Não é metabolizado por rins ou fígado.
Segurança pré-clínica
Em animais: pode afetar desenvolvimento ósseo em crescimento, cicatrização e fertilidade feminina. Não afeta pressão arterial, função renal ou hemostasia.

 Revisado clinicamente por: Isabelle Baião de Mello Neto (CRF-MG 24309). Atualizado em: 01 de outubro de 2025.
Revisado clinicamente por: Isabelle Baião de Mello Neto (CRF-MG 24309). Atualizado em: 01 de outubro de 2025.