Qual a ação da substância do Becenun?
Resultados de Eficácia
Cirurgia Primária
Em estudo clínico randomizado, duplo-cego, placebo-controlado conduzido em 240 pacientes adultos com glioma de alto grau de malignidade recentemente diagnosticado submetidos à craniotomia inicial para ressecção do tumor (Estudo 1), a sobrevida mediana foi aumentada de 11,6 meses com placebo para 13,9 meses com o implante de carmustina Carmustina (valor-p 0.079, não estratificado teste log-rank) na fase do estudo original.
O placebo utilizado era um implante sem carmustina, mas com a mesma matriz polimérica do medicamento em estudo.
A população no Estudo 1 foi 67% do sexo masculino, 97% brancos, a idade mediana foi 53 anos (variação: 21 – 72). No Estudo 1, 87% tinham um performance status de Karnofsky ≥ 70 e 71% tinham um performance status de Karnofsky de ≥ 80%. No Estudo 1, 78% tinham o subtipo histológico de glioblastoma multiforme como determinado pela revisão de patologia central. E 38% dos pacientes receberam 8 implantes e 78% receberam ≥ 6 implantes. Começando 3 semanas após a cirurgia, 80% dos pacientes receberam terapia de radiação de campo limitado padrão (RT) descrito como 55 – 60 Gy em 28 a 30 frações ao longo de 6 semanas; um adicional de 11% não recebeu nenhuma radioterapia e o restante recebeu radioterapia não padrão ou uma combinação de radioterapia padrão e não padrão. No momento da progressão, 24% receberam quimioterapia sistêmica.
Ocorreram mortes dentro de 30 dias da implantação em 5 pacientes (4%) recebendo Carmustina comparado a 2 pacientes (2%) recebendo placebo. As mortes no braço Carmustina resultaram de hematoma/edema cerebral (n = 3), embolismo pulmonar (n = 1) e evento coronário agudo (n = 1). As mortes no braço placebo resultaram de sepse (n = 1) e doença maligna (n = 1).
Tabela 1: Sobrevida Global em Pacientes com Glioma Recentemente Diagnosticado, Estudo 1:
| Sobrevida Global – ITT* | Carmustina (n = 120) | Placebo Implante (n = 120) |
| Número de mortes, n (%) | 111 (93%) | 117 (98%) |
| Sobrevida global mediana, meses (95% CI) | 13.9 (12.1, 15.1) | 11.6 (10.2, 12.7) |
| Razão de risco (95% CI) | 0.73 (0.56, 0.95) | |
| Test Log-Rank valor-p | < 0.02** | |
*Baseado na análise final, teste log-rank não estratificado especificado no protocolo.
**Valor-p não ajustado par comparações múltiplas.
Figura 1: Sobrevida Global para Pacientes com Glioma de Alto Grau de Malignidade Recentemente Diagnosticado – Curvas Kaplan-Meier por Grupo de Tratamento*
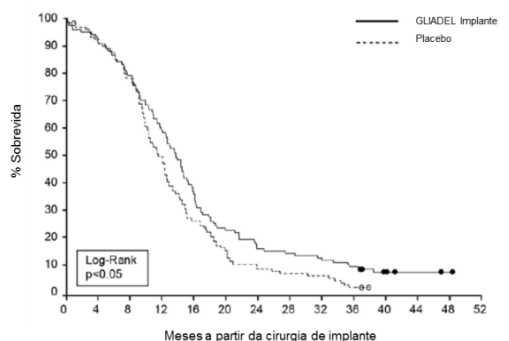
*Baseado na análise final, teste log-rank não estratificado especificado no protocolo; valor-p não ajustado par comparações múltiplas.
Glioblastoma Multiforme Recorrente
A segurança de Carmustina foi avaliada em um estudo multicêntrico, randomizado (1:1), duplo-cego, placebo controlado de 222 pacientes com glioma de alto grau de malignidade recorrente que receberam até 8 Carmustina ou placebo correspondente, implantados contra as superfícies da ressecção após a ressecção máxima do tumor (Estudo 2). Era solicitado que os pacientes tivessem recebido previamente terapia de radiação de feixe externo suficiente para desqualificá-los de terapia de radiação adicional. Todos os pacientes foram elegíveis para receber quimioterapia que foi suspensa por pelo menos 4 semanas (6 para nitrosoureias) antes e 2 semanas após a cirurgia.
A população no Estudo 2 era de 64% do sexo masculino, 92% brancos, e tinha uma idade mediana de 49 anos (variação: 19 – 80). No Estudo 2, 65% tinham subtipo histológico de glioblastoma multiforme, 26% tinham astrocitoma anaplástico ou outra variante anaplástica, 73% tinham um performance status de Karnofsky ≥ 70, 53% tinham um performance status de Karnofsky de ≥ 80%, 73% tinham somente uma cirurgia prévia, e 46% tinham tratamento prévio com nitrosoureia. No Estudo 2, 81% dos pacientes receberam 8 implantes e 96% receberam ≥ 6 implantes.
No Estudo 2, 64 reações adversas graves foram relatadas em 43 pacientes (39%) recebendo Carmustina. As reações adversas observadas nos pacientes tratados com Carmustina estão na Seção 9. REAÇÕES ADVERSAS. Meningite ocorreu em 4 pacientes recebendo Carmustinas e em nenhum dos pacientes recebendo placebo.
Meningite bacteriana foi confirmada em 2 pacientes:
- O primeiro com início quatro dias após a implantação de Carmustina; o Segundo após ressecção para recorrência do tumor 155 dias após a implantação de Carmustina. Um caso, atribuído à meningite química resolveu após tratamento com esteroide. A causa do quarto caso foi indeterminada, mas resolveu após tratamento com antibiótico.
As taxas de sobrevida e mortalidade em 6 meses no subgrupo de pacientes com glioblastoma multiforme recorrente foram medidas de desfecho exploratórias e estão resumidas na Tabela 2 e Figuras 2 e 3. Não foi observado prolongamento da sobrevida em pacientes com diagnósticos patológicos diferentes de glioblastoma multiforme.
Tabela 2: Principais medidas de desfecho de eficácia em pacientes com glioblastoma multiforme recorrente, Estudo 2:
| --- | Carmustina | Placebo |
| Glioblastoma multiforme | n = 72 | n = 73 |
| Sobrevida em 6 Meses | ||
| Número de mortes, n (%) | 32 | 47 |
| Taxa de sobrevida em 6 meses (%) | 56% | 36% |
| Valor-p do teste Log-Rank | 0,013** | |
| Valor-p do teste Gehan’s generalized Wilcoxon | 0,015** | |
| Sobrevida global | ||
| Número de mortes, n (%) | 71 (99%) | 72 (99%) |
| Mediana da sobrevida global (95% CI) (meses) | 6,51 (5,32; 7,49) | 4,63 (3,78; 5,52) |
| Valor-p do teste Log-Rank | 0,181** | |
| Valor-p do teste Gehan’s generalized Wilcoxon | 0,021** | |
**Valor-p não ajustado para comparações múltiplas.
Figura 2: Sobrevida em 6 Meses para Pacientes com Glioblastoma Multiforme Recorrente – Curvas de Kaplan-Meier por Grupo de Tratamento:
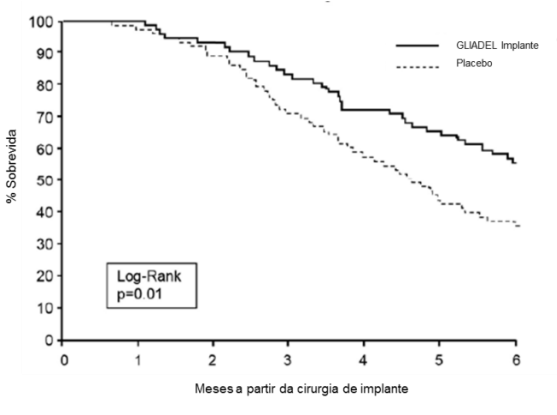
Figura 3: Sobrevida Global (meses) para Pacientes com Glioblastoma Multiforme Recorrente – Curvas de Kaplan-Meier por grupo de tratamento:
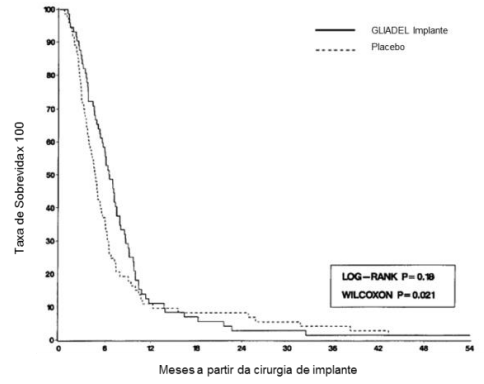
Referências Bibliográficas:
1. Estudo 1: Westphal, M., Hilt, D.C., Bortey, E., Delavault, P., Olivares, R., Warnke, P.C., Whittle, l.R., Jaaskelainen, J., and Ram, Z. (2003) A phase 3 trial of local chemotheraphy with biodegradable carmustine (BCNU) wafers (Carmustina wafers) in patients with primary malignant glioma. Neuro- Oncology [serial online], Doc. 02-023, February 10, 2003. URL http://neurooncology.mc.duke.edu - A phase 3 trial of local chemotherapy with biodegradable carmustine (BCNU) wafers (Carmustina wafers) in patients with primary malignant glioma.
2. Estudo 2: Brem, H., Piantadosi, S., Burger, P.C., Walker, M., Selker, R., Vick, N.A., Black, K., Sisti, M., Brem, S., Mohr, G., Muller, P., Morawetz, R., Schold, S.C. (1995) Placebo-controlled trial of safety and efficacy of intraoperative controlled delivery by biodegradable polymers of chemotherapy for recurrent gliomas. Lancet; 345, No. 8956, p1008-1012, April 22, 1995. URL http://www.thelancet.com/journals/lancet/article/PIIS0140-6736(95)90755-6/abstract - Placebo-controlled trial of safety and efficacy of intraoperative controlled delivery by biodegradable polymers of chemotherapy for recurrent gliomas.
Características Farmacológicas
Farmacodinâmica
Carmustina foi desenhado para difundir carmustina diretamente na cavidade cirúrgica criada quando um tumor cerebral é ressectado. Na exposição ao ambiente aquoso da cavidade da ressecção, as ligações anidrido no copolímero são hidrolisadas, liberando carmustina, carboxifenoxipropano, e ácido sebácico. A carmustina liberada do implante Carmustina difunde no tecido cerebral circundante e produz um efeito antineoplásico pela alquilação de DNA e RNA.
A carmustina mostrou degradar tanto espontaneamente quanto metabolicamente. A produção de uma entidade alquilante, hipoteticamente um íon cloroetil carbônio, leva à formação de ligações cruzadas de DNA.
A atividade tumoricida de Carmustina é dependente da liberação da carmustina na cavidade do tumor em concentrações suficientes para citotoxicidade efetiva.
Mais que 70% do copolímero degrada-se em 3 semanas. A disposição metabólica e excreção dos monômeros diferem. O carboxifenoxipropano é eliminado pelo rim e ácido sebácico, um ácido graxo endógeno, é metabolizado pelo fígado e eliminado como CO2 em animais.
Farmacocinética
A absorção, distribuição, metabolismo e excreção do copolímero em humanos são desconhecidos. As concentrações de carmustina liberadas pelo Carmustina no tecido do cérebro humano não foram determinadas. Os níveis plasmáticos de carmustina após Carmustina ser implantado não foram determinados. Em coelhos que receberam implantes contendo 3,85% de carmustina, não foram encontrados níveis detectáveis de carmustina no plasma ou fluido cérebro-espinhal.
Após uma infusão intravenosa de carmustina em doses variando de 30 a 170 mg/m2, a meia-vida terminal, clearance (depuração), e volume de distribuição no estado de equilíbrio foram 22 minutos, 56 mL/min/kg, e 3,25 L/kg, respectivamente. Aproximadamente 60% da dose intravenosa de 200 mg/m2 de 14C-carmustina foram excretados na urina ao longo de 96 horas e 6% foram eliminadas como CO2.
Os implantes de Carmustina são biodegradáveis no cérebro humano quando inseridos na cavidade após a ressecção do tumor. A taxa de biodegradação é variável de paciente para paciente.

 Revisado por Isabelle Baião de Mello Neto (CRF-MG 24309)
Revisado por Isabelle Baião de Mello Neto (CRF-MG 24309)