Para que serve o Arava?
Arava é usado para tratar artrite reumatoide ativa (inflamação crônica das juntas), diminuindo os sinais e sintomas, impedindo a destruição das juntas e ajudando a melhorar as funções físicas e a qualidade de vida. Arava também é usado para artrite psoriásica ativa (doença inflamatória que afeta alguns pacientes com psoríase crônica na pele).
Como o Arava age no corpo?
A leflunomida é um remédio para reumatismo que modifica a doença e tem ação antiproliferativa. Ela demonstrou melhorar os sinais e sintomas e reduzir a progressão da destruição das juntas na artrite reumatoide ativa.
A leflunomida é transformada rapidamente em sua substância ativa (A771726), responsável por todo o efeito terapêutico do remédio Arava.
Os resultados do tratamento podem aparecer após 4 semanas e continuar melhorando entre 4 e 6 meses após o início.
Quem não pode tomar Arava?
Arava não deve ser usado por pacientes com alergia ou intolerância à leflunomida, teriflunomida ou qualquer componente da fórmula. Também é contraindicado para mulheres grávidas ou que possam engravidar sem usar métodos contraceptivos confiáveis, ou que após o tratamento ainda tenham concentração da substância ativa (A771726) acima de 0,02 mg/L.
A gravidez deve ser descartada antes de começar o tratamento. Em caso de dúvida, converse com seu médico.
Este remédio não deve ser usado por mulheres grávidas ou que possam engravidar durante o tratamento.
Como tomar Arava?
Tome os comprimidos inteiros com líquido, por via oral.
O tratamento com Arava deve ser iniciado e acompanhado por médicos experientes em artrite reumatoide.
Para artrite reumatoide, o tratamento geralmente começa com uma dose inicial de 100 mg uma vez ao dia por 3 dias. Pular a dose inicial pode reduzir o risco de efeitos colaterais. A dose de manutenção é de 20 mg de Arava uma vez ao dia. Se a dose de 20 mg não for bem tolerada, o médico pode reduzir.
Para artrite psoriásica, também se inicia com 100 mg uma vez ao dia por 3 dias, seguido de 20 mg de Arava uma vez ao dia.
Os resultados podem ser vistos após 4 semanas e melhorar entre 4 e 6 meses. O tratamento com Arava geralmente é longo.
Não há estudos sobre o uso de Arava por outras vias. Por segurança, use apenas por via oral, conforme orientação médica.
Grupos específicos
Crianças e Adolescentes
Arava não é recomendado para menores de 18 anos, pois segurança e eficácia não foram estabelecidas.
Idosos
Não é necessário ajuste de dose para maiores de 65 anos.
Pacientes com problemas nos rins ou fígado
Use com cautela neste grupo.
Siga as orientações do seu médico sobre horários, doses e duração do tratamento. Não pare o tratamento sem orientação médica.
Não parta ou mastigue este remédio.
O que fazer se esquecer de tomar Arava?
Se esquecer uma dose, tome assim que lembrar. Se estiver perto da próxima dose, espere e mantenha o intervalo normal. Nunca tome duas doses juntas.
Em caso de dúvida, procure orientação do farmacêutico ou médico.
Precauções ao usar Arava
Geral
Devido ao longo tempo de ação da substância ativa, efeitos colaterais podem ocorrer mesmo após parar o tratamento.
Em caso de efeito colateral grave, procure atendimento médico para tomar colestiramina ou carvão ativado, repetindo se necessário. Em reações alérgicas graves, pode ser necessário prolongar esse tratamento para eliminar o remédio rapidamente.
Não use teriflunomida com leflunomida, pois a leflunomida origina a teriflunomida.
Fígado
Use com cautela em pacientes com problemas no fígado devido ao risco de toxicidade hepática. Não é recomendado para pacientes com insuficiência hepática significativa ou doença hepática pré-existente.
Seu médico fará exames de função hepática antes e durante o tratamento.
Seu médico pode ajustar a dose se sua função hepática estiver alterada:
Se as enzimas hepáticas estiverem 2 a 3 vezes acima do normal, a dose pode ser reduzida de 20 mg para 10 mg/dia, com monitoramento cuidadoso.
Se as enzimas permanecerem elevadas ou ultrapassarem 3 vezes o limite, pare o tratamento e use colestiramina ou carvão ativado.
Raros casos de dano hepático grave foram relatados, principalmente nos primeiros 6 meses. Siga rigorosamente as recomendações de monitoramento.
Sangue e sistema imunológico
O risco de reações sanguíneas aumenta em pacientes com anemia, baixos glóbulos brancos ou plaquetas, problemas na medula óssea ou risco de supressão da medula.
Antes do tratamento, seu médico fará hemograma completo, repetindo mensalmente nos primeiros 6 meses e depois a cada 6-8 semanas.
Converse com seu médico sobre a necessidade de exames de sangue frequentes se:
- Usar ou ter usado remédios imunossupressores ou tóxicos para o sangue;
- Ter histórico de problemas sanguíneos;
- Apresentar alterações sanguíneas no início do tratamento não relacionadas à artrite.
Consulte a seção "Superdose" para ações em reações sanguíneas graves.
Não é recomendado para pacientes com:
- Imunodeficiência grave (ex: AIDS);
- Problemas significativos na medula óssea;
- Infecções graves.
Infecções
Remédios como leflunomida podem aumentar a suscetibilidade a infecções, incluindo oportunistas. Infecções podem ser mais graves e exigir tratamento precoce. Procure seu médico em caso de infecção grave, pois pode ser necessário parar o tratamento.
Remédios imunossupressores podem ativar tuberculose. Médicos devem estar atentos para diagnóstico e tratamento precoces.
Antes do tratamento, todos os pacientes devem ser avaliados para tuberculose. Pacientes com histórico de tuberculose devem ser monitorados cuidadosamente.
Sistema respiratório
Informe seu médico se tiver histórico de doença pulmonar intersticial ou sintomas como tosse e falta de ar. Raramente ocorreu doença pulmonar intersticial durante o tratamento. O risco aumenta com histórico dessa doença. Sintomas pulmonares podem exigir parada do tratamento e investigação.
Nervos periféricos
Foram relatados casos de neuropatia periférica. A maioria melhorou após parar a leflunomida. Idade acima de 60 anos, uso de remédios neurotóxicos e diabetes podem aumentar o risco. Procure seu médico rapidamente se desenvolver neuropatia periférica.
Rins
Não há dados suficientes para recomendar ajuste de dose em pacientes com problemas nos rins. Use com cautela.
Reações na pele
Casos de síndrome de Stevens-Johnson, necrólise epidérmica tóxica e reação com eosinofilia foram relatados. Se desenvolver qualquer uma dessas condições, procure médico imediatamente.
Úlceras na pele podem ocorrer. Se suspeitar de úlcera relacionada à leflunomida ou se não melhorar com tratamento, pare o remédio e inicie procedimento de eliminação.
Informe seu médico se desenvolver úlcera na pele durante o tratamento.
Pressão arterial
Converse com seu médico sobre monitoramento da pressão durante o tratamento. A pressão deve ser verificada antes e periodicamente.
Abuso e dependência
Não se conhece potencial de abuso ou dependência.
Gravidez e amamentação
Devido ao risco de malformação fetal, descarte gravidez antes e durante o tratamento, e até 2 anos após o fim. Arava é contraindicado na gravidez ou em mulheres que possam engravidar sem método contraceptivo eficaz. Informe qualquer suspeita de gravidez durante o tratamento ou até 2 anos após o uso.
Para mulheres que desejam engravidar, recomenda-se:
- Após parar o tratamento, tomar 8 g de colestiramina, 3 vezes ao dia, por 11 dias; ou
- Após parar o tratamento, tomar 50 g de carvão ativado, 4 vezes ao dia, por 11 dias.
Não é necessário fazer isso em 11 dias consecutivos, exceto se precisar reduzir rapidamente a concentração do remédio.
A concentração deve estar abaixo de 0,02 mg/L, confirmada por dois testes com intervalo mínimo de 14 dias.
Concentrações abaixo de 0,02 mg/L têm risco mínimo.
Sem o procedimento de eliminação, podem ser necessários até 2 anos para alcançar níveis seguros.
Mesmo após esse período, verifique se os níveis estão abaixo de 0,02 mg/L.
Se não puder esperar 2 anos após o tratamento, use métodos contraceptivos confiáveis e adote os procedimentos de eliminação.
Contraceptivos orais podem não funcionar durante os procedimentos de eliminação. Use métodos alternativos.
Seu médico tem informações sobre o risco de malformação fetal.
Amamentação
A leflunomida passa para o leite materno. Não amamente durante o tratamento.
Informe seu médico se estiver amamentando.
Dirigir e operar máquinas
Não há informações relevantes sobre os efeitos de Arava nessa capacidade.
Efeitos colaterais do Arava
- Muito comum (ocorre em mais de 10% dos pacientes).
- Comum (ocorre entre 1% e 10% dos pacientes).
- Incomum (ocorre entre 0,1% e 1% dos pacientes).
- Raro (ocorre entre 0,01% e 0,1% dos pacientes).
- Muito raro (ocorre em menos de 0,01% dos pacientes).
- Desconhecido (não pode ser estimado com dados disponíveis).
Sistema digestivo e fígado
- Comum: diarreia, náusea, vômitos, perda de apetite, problemas na boca (ex: aftas, feridas), dor abdominal, aumento de enzimas hepáticas, colite;
- Raro: hepatite, icterícia/redução do fluxo biliar;
- Muito raro: dano hepático grave, insuficiência hepática, morte de células do fígado (pode ser fatal), inflamação no pâncreas.
Sistema cardiovascular
- Comum: aumento da pressão arterial;
- Desconhecido: aumento da pressão nos pulmões.
Sangue e sistema linfático
- Comum: redução de glóbulos brancos;
- Incomum: anemia, redução de plaquetas;
- Raro: redução grave de glóbulos brancos, aumento de eosinófilos, redução global de células sanguíneas.
Uso recente de agentes tóxicos para a medula óssea pode aumentar o risco de efeitos sanguíneos.
Sistema nervoso
- Comum: dor de cabeça, tontura, formigamento;
- Incomum: alteração do paladar, ansiedade;
- Muito raro: doença nos nervos periféricos.
Reações alérgicas e pele
- Comum: reações alérgicas leves (ex: vermelhidão), coceira, eczema, pele seca, queda de cabelo;
- Incomum: urticária;
- Muito raro: reações alérgicas graves, síndrome de Stevens-Johnson, necrólise epidérmica tóxica, inflamação dos vasos sanguíneos.
Infecções
- Raro: infecções graves e sepse, que podem ser fatais.
A maioria dos casos teve outros fatores de risco. Remédios como leflunomida podem aumentar a suscetibilidade a infecções.
Em estudos, rinite, bronquite e pneumonia foram levemente mais frequentes com leflunomida versus placebo.
Pulmões e tórax
- Raro: doença pulmonar intersticial, que pode ser fatal.
Pele e tecido subcutâneo
- Desconhecido: lúpus cutâneo, psoríase pustulosa ou piora da psoríase, reação com eosinofilia, úlcera na pele.
Outras reações
- Comum: perda de peso, fraqueza;
- Incomum: redução de potássio no sangue.
Pode ocorrer aumento leve de gordura no sangue. Os níveis de ácido úrico geralmente diminuem.
Outras alterações laboratoriais:
- Pequenos aumentos de LDH e creatina quinase; pequenas reduções de fosfato.
Foram relatados casos de inflamação e ruptura de tendão, mas não foi estabelecida relação causal.
Pequena redução reversível na concentração, contagem total e motilidade de espermatozoides não pode ser descartada.
O risco de câncer, especialmente distúrbios linfoproliferativos, pode aumentar com imunossupressores.
Informe seu médico, dentista ou farmacêutico sobre qualquer efeito indesejado.
Uso em grupos especiais (idosos, crianças, etc.)
Homens
As informações disponíveis não indicam risco de toxicidade fetal mediada pelo pai. Homens que desejam ter filhos devem considerar parar o tratamento e usar procedimento de eliminação.
Idosos
Não é necessário ajuste de dose em maiores de 65 anos.
Crianças e Adolescentes
Segurança e eficácia não foram estabelecidas; não recomendado para menores de 18 anos.
Apresentações do Arava
Comprimido Revestido
- Embalagem com 30.
- Embalagem com 3.
Uso oral.
Uso adulto.
Composição do Arava
Cada comprimido revestido de 20 mg contém:
20 mg de leflunomida.
Excipientes: lactose monoidratada, amido de milho, povidona K25, dióxido de silício, estearato de magnésio, crospovidona, hipromelose, macrogol 8000, dióxido de titânio, óxido férrico amarelo e talco.
Cada comprimido revestido de 100 mg contém:
100 mg de leflunomida.
Excipientes: lactose monoidratada, amido de milho, povidona K25, dióxido de silício, estearato de magnésio, crospovidona, hipromelose, macrogol 8000, dióxido de titânio e talco.
Superdose de Arava: sintomas e tratamento
Sinais e Sintomas
Foram relatados casos de superdose crônica (5 vezes a dose diária recomendada) e superdose aguda em adultos e crianças. A maioria não teve eventos adversos. Quando ocorreram, foram consistentes com o perfil de segurança: diarreia, dor abdominal, redução de glóbulos brancos, anemia e aumento de enzimas hepáticas.
Procedimento em caso de superdose
Em caso de superdose, recomenda-se tomar colestiramina ou carvão ativado para acelerar a eliminação. Tomar colestiramina (8 g, três vezes ao dia por 24 horas) reduziu os níveis em 40% nas primeiras 24 horas. Carvão ativado (50 g a cada 6 horas por 24 horas) reduziu em 37% em 24 horas.
Esses procedimentos podem ser repetidos se necessário. Hemodiálise não remove o metabólito ativo.
Em caso de superdose, procure socorro médico e leve a embalagem. Ligue para 0800 722 6001 para orientações.
Interações com outros remédios
Se já estiver usando anti-inflamatórios não esteroides (AINEs) e/ou corticosteroides em baixas doses, pode continuar após iniciar Arava.
Pode aumentar efeitos colaterais se usar recentemente ou junto com substâncias tóxicas para fígado (incluindo álcool), sangue ou imunossupressoras.
Metotrexato
Em estudo com coadministração, alguns pacientes tiveram aumento de enzimas hepáticas. Monitore cuidadosamente as enzimas hepáticas ao substituir leflunomida por metotrexato.
Vacinas
Não use vacinas vivas atenuadas durante o tratamento. Considere a meia-vida longa da leflunomida ao vacinar após parar o tratamento.
Varfarina
Foram relatados casos de aumento do tempo de coagulação. Monitore cuidadosamente a RNI (Razão Normalizada Internacional) ao usar com varfarina.
Alimentos
A absorção não é afetada por alimentos.
Efeito de outros remédios sobre a leflunomida
Estudos sugerem que enzimas CYP1A2, 2C19 e 3A4 estão envolvidas no metabolismo. Rifampicina pode aumentar os níveis. Colestiramina ou carvão ativado reduzem rapidamente as concentrações.
Efeito da leflunomida sobre outros remédios
Substratos da BCRP
Não houve interação com metotrexato. Não foi demonstrada interação significativa com contraceptivos orais trifásicos.
Considere os seguintes resultados:
Repaglinida (substrato CYP2C8)
Aumento nos níveis de repaglinida. Monitore pacientes usando remédios metabolizados por CYP2C8 (repaglinida, paclitaxel, pioglitazona, rosiglitazona).
Cafeína (substrato CYP1A2)
Redução nos níveis de cafeína. Use com precaução remédios metabolizados por CYP1A2 (duloxetina, alosetrona, teofilina, tizanidina).
Substratos do transportador OAT3
Aumento nos níveis de cefaclor. Use com cautela com substratos de OAT3 (cefaclor, benzilpenicilina, ciprofloxacino, indometacina, cetoprofeno, furosemida, cimetidina, metotrexato, zidovudina).
Substratos da BCRP e/ou OATP1B1/B3
Aumento nos níveis de rosuvastatina. Dose de rosuvastatina não deve exceder 10 mg/dia. Use com cautela com outros substratos (metotrexato, topotecana, sulfassalazina, daunorrubicina, doxorrubicina, sinvastatina, atorvastatina, pravastatina, nateglinida, repaglinida, rifampicina).
Contraceptivo oral (etinilestradiol e levonorgestrel)
Aumento nos níveis do contraceptivo. Tome precauções dependendo do tipo de contraceptivo.
Varfarina
Redução de 25% no pico da RNI. Monitore cuidadosamente a RNI.
Uso concomitante com antimaláricos (cloroquina, hidroxicloroquina), ouro, D-penicilamina, azatioprina e outros imunossupressores (ciclosporina, metotrexato) não foi adequadamente estudado.
Informe seu médico sobre qualquer outro remédio que esteja usando.
Não use remédio sem conhecimento do seu médico. Pode ser perigoso.
Tomar Arava com alimentos
A absorção não é afetada por alimentos.
Como o Arava age no organismo?
Resultados de Eficácia
Artrite Reumatoide
A eficácia da leflunomida foi demonstrada em três estudos, mostrando redução de sinais/sintomas e inibição de danos nas juntas. Em dois estudos, também melhorou a função física. Todos usaram dose inicial de 100 mg/dia por três dias, seguida de 20 mg/dia.
US301
Estudo placebo-controlado de 2 anos com 482 pacientes. Após 52 semanas, 52,2% no grupo leflunomida tiveram resposta ACR20 vs 26,3% no placebo.
MN301/303/305
Estudo placebo-controlado de 24 semanas com 358 pacientes. Após 6 meses, 54,6% no grupo leflunomida tiveram resposta ACR20 vs 28,6% no placebo.
MN302/304
Estudo ativo-controlado (sem placebo) de 52 semanas com 999 pacientes. Após 12 meses, 51,1% no grupo leflunomida tiveram resposta ACR20 vs 65,2% no metotrexato.
Sinais e Sintomas
Avaliados pelo índice ACR20. Leflunomida foi superior ao placebo em redução de sinais/sintomas. O efeito apareceu após 1 mês, estabilizou entre 3-6 meses e continuou. Respostas ACR50 e ACR70 também foram melhores.
Figura 1: Taxas de resposta ACR no desfecho
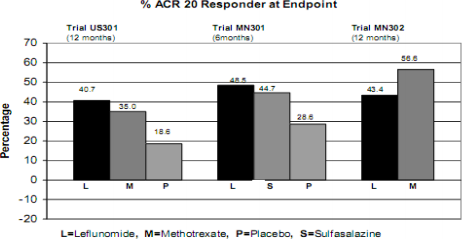
| - | Comparações | Intervalo de Confiança | Valor p |
US301 | Leflunomida vs. Placebo | (12, 32) | < 0,0001 |
Metotrexato vs. Placebo | (8, 30) | < 0,0001 | |
Leflunomida vs. Metotrexato | (-4, 16) | NS | |
MN301 | Leflunomida vs. Placebo | (7, 33) | 0,0026 |
Sulfassalazina vs. Placebo | (4, 29) | 0,0121 | |
Leflunomida vs. Sulfassalazina | (-8, 16) | NS | |
MN302 | Leflunomida vs. Metotrexato | (-19, -7) | < 0,0001 |
Figura 2: Percentual de pacientes com resposta ACR20 ao longo do tempo*
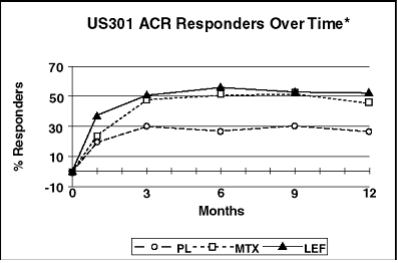
*Última observação realizada.
Tabela 1: Resumo das Taxas de Resposta ACR*
Grupo de Estudo e Tratamento | ACR20 | ACR50 | ACR70 |
Estudos Placebo-Controlados | |||
US301 (12 meses) | |||
Leflunomida (n=178)† | 52,2‡ | 34,3‡ | 20,2‡ |
Placebo (n=118)† | 26,3 | 7,6 | 4,2 |
Metotrexato (n=180)† | 45,6 | 22,8 | 9,4 |
MN301 (6 meses) | |||
Leflunomida (n=130)† | 54,6‡ | 33,1‡ | 10,0§ |
Placebo (n=91)† | 28,6 | 14,3 | 2,2 |
Sulfassalazina (n=132)† | 56,8 | 30,3 | 7,6 |
Estudos sem grupo placebo | |||
MN302 (12 meses) | |||
Leflunomida (n=495)† | 51,1 | 31,1 | 9,9 |
Metotrexato (n=489)† | 65,2 | 43,8 | 16,4 |
*Análise por intenção de tratamento (ITT) utilizando a técnica da Última Observação Realizada (LOCF), para pacientes que interromperam o tratamento precocemente.
† N é o número de pacientes ITT para os quais havia dados adequados disponíveis para cálculo das taxas indicadas.
‡ p > 0,001 leflunomida vs. placebo.
§ p > 0,02 leflunomida vs. placebo.
Tabela 2: Alteração Média nos Componentes do Índice ACR*:
Componentes | Estudos Placebo-Controlados | Estudo Não-Placebo Controlado | ||||||
| --- | US301 (12 meses) | MN301 - Não-EUA (6 meses) | MN302 - Não-EUA (12 meses) | |||||
| --- | Leflunomida | Metotrexato | Placebo | Leflunomida | Sulfassalazina | Placebo | Leflunomida | Metotrexato |
Contagem de articulação dolorosa1 | -7,7 | -6,6 | -3,0 | -9,7 | -8,1 | -4,3 | -8,3 | -9,7 |
Contagem de articulação tumefacta1 | -5,7 | -5,4 | -2,9 | -7,2 | -6,2 | -3,4 | -6,8 | -9,0 |
Avaliação global do paciente2 | -2,1 | -1,5 | 0,1 | -2,8 | -2,6 | -0,9 | -2,3 | -3,0 |
Avaliação global do médico2 | -2,8 | -2,4 | -1,0 | -2,7 | -2,5 | -0,8 | -2,3 | -3,1 |
Função física /desabilidade (MHAQ/HAQ) | -0,29 | -0,15 | 0,07 | -0,50 | -0,29 | -0,04 | -0,37 | -0,44 |
Intensidade da dor2 | -2,2 | -1,7 | -0,5 | -2,7 | -2,0 | -0,9 | -2,1 | -2,9 |
Taxa de sedimentação eritrocitária | -6,26 | -6,48 | 2,56 | -7,48 | -16,56 | 3,44 | -10,12 | -22,18 |
Proteína C-reativa | -0,62 | -0,50 | 0,47 | -2,26 | -1,19 | 0,16 | -1,86 | -2,45 |
Não incluído no Índice ACR | ||||||||
Rigidez matinal (min) | -101,4 | -88,7 | 14,7 | -93,0 | -42,4 | -6,8 | -63,7 | -86,6 |
* Última observação realizada; Alterações negativas indicam melhoras.
1 Com base na contagem de 28 articulações.
2 Escala Visual Analógica: 0 = Melhor; 10 = Pior.
Inibição do dano estrutural
Avaliada pelo Escore Sharp (erosões e redução do espaço articular). Leflunomida foi superior ao placebo na inibição da progressão da doença.
Figura 3: Alteração média no Escore Sharp total*
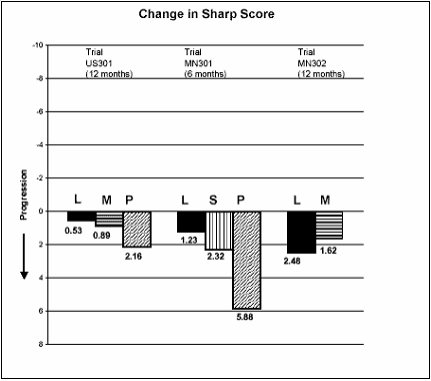
L = leflunomida.
M = metotrexato.
S = sulfassalazina.
P = placebo.
Comparações | Intervalo de Confiança 95% | Valor p | |
US301 | Leflunomida vs. Placebo | (-4,0 , -1,1) | 0,0007 |
Metotrexato vs. Placebo | (-2,6 , -0,2) | 0,0196 | |
Leflunomida vs. Metotrexato | (-2,3 , 0,0) | 0,0499 | |
MN301 | Leflunomida vs. Placebo | (-6,2 , -1,8) | 0,0004 |
Sulfassalazina vs. Placebo | (-6,9 , 0,0) | 0,0484 | |
Leflunomida vs. Sulfassalazina | (-3,3 , 1,2) | NS | |
MN302 | Leflunomida vs. Metotrexato | (-2,2 , 7,4) | NS |
Melhora na função física
Avaliada pelo HAQ (Questionário de Avaliação de Saúde). Leflunomida foi superior ao placebo na melhora da função física.
Figura 4: Alteração média no HAQ DI*
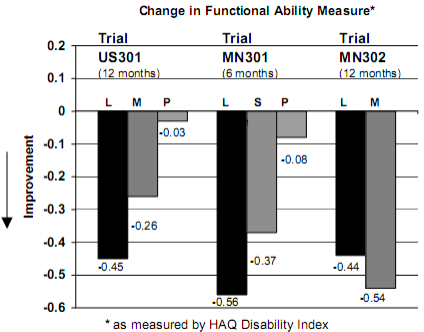
L = leflunomida.
M = metotrexato.
S = sulfassalazina.
P = placebo.
Comparações | Intervalo de Confiança 95% | Valor p | |
US301 | Leflunomida vs. Placebo | (-0,58 , -0,29) | 0,0001 |
Leflunomida vs. Metotrexato | (-0,34 , -0,07) | 0,0026 | |
MN301 | Leflunomida vs. Placebo | (-0,67 , -0,36) | < 0,0001 |
Leflunomida vs. Sulfassalazina | (-0,33 , -0,03) | 0,0163 | |
MN302 | Leflunomida vs. Metotrexato | (0,01 , 0,16) | 0,0221 |
Artrite Psoriásica
Estudo de 6 meses com leflunomida vs placebo. 59,0% no grupo leflunomida tiveram resposta PsARC vs 29,7% no placebo (p<0,0001). Também houve melhora significativa nos escores PASI (avaliação de psoríase).
Tabela 3: Alteração Média nos Componentes do Índice PsARC*
Componentes | Estudo placebo-controlado (6 meses) | ||
| --- | Leflunomida (n=95) | Placebo (n=91) | Valores de p |
Escore de articulação dolorosa* | -9,1 | -4,6 | 0,0022 |
Escore de articulação tumefacta* | -6,8 | -4,2 | 0,0013 |
Avaliação global do médico – com melhora em pelo menos uma categoria1 | 52,6% | 34,1% | < 0,0001 |
Auto-avaliação global do paciente – com melhora em pelo menos uma categoria1 | 31,6% | 30,8% | 0,0036 |
* Alterações negativas indicam melhoras.
1 escala Likert de 5 pontos: 1 = Muito bom; 5 = Muito pobre.
Gravidez
Estudo prospectivo mostrou defeitos congênitos em 5,4% dos nascidos vivos após exposição inadvertida no primeiro trimestre (vs 4,2% nos grupos controle). O estudo não altera a contraindicação.
Estudos pós-comercialização
Estudo com pacientes virgens de tratamento com DMARD não mostrou benefício adicional com dose inicial de ataque. A resposta ACR20 foi 58,5% com dose de ataque vs 77,8% sem (p = 0,025).
Características Farmacológicas
Farmacodinâmica
A leflunomida é um agente antirreumático com propriedades antiproliferativas. Seu metabólito ativo (A771726) inibe a enzima di-hidroorotato desidrogenase (DHODH), reduzindo a síntese de pirimidina em linfócitos e outras células de divisão rápida.
Farmacocinética
A leflunomida é rapidamente convertida em A771726. Após dose única, o pico plasmático de A771726 ocorre entre 1-24 horas. A absorção não é afetada por alimentos. A dose de manutenção é 20 mg/dia, com concentração plasmática média de 35 µg/mL. Ligação às proteínas plasmáticas é extensa (≈99,4%). Meia-vida de eliminação é ≈2 semanas. Eliminada por metabolismo hepático e excreção biliar/fecal. Pacientes com problemas renais ou hepáticos requerem cautela.
Como guardar o Arava?
Guarde Arava em temperatura ambiente (15 a 30°C), na embalagem original bem fechada.
Número de lote e datas de fabricação/validade: veja na embalagem.
Não use após o vencimento. Guarde na embalagem original.
Características
- Arava 20 mg: Comprimidos triangulares esféricos, amarelados a ocre, com "ZBO".
- Arava 100 mg: Comprimidos redondos biconvexos, brancos, com "ZBP".
Antes de usar, observe o aspecto do remédio. Se houver mudança, consulte o farmacêutico.
Mantenha fora do alcance de crianças.
Alertas importantes sobre Arava
Risco para gravidez. Pode causar má formação fetal.
Informações legais do Arava
MS 1.8326.0442
Farm. Resp.:
Ricardo Jonsson
CRF-SP: 40.796
Registrado e importado por:
Sanofi Medley Farmacêutica Ltda.
Rua Conde Domingos Papaiz, 413 - Suzano– SP
CNPJ 10.588.595/0010-92
Indústria Brasileira
®Marca Registrada
Fabricado por:
Opella Healthcare International SAS
56, route de Choisy
60200 – Compiègne – França
Venda sob prescrição médica.
Só pode ser vendido com retenção de receita.

 Revisado clinicamente por: Isabelle Baião de Mello Neto (CRF-MG 24309). Atualizado em: 01 de outubro de 2025.
Revisado clinicamente por: Isabelle Baião de Mello Neto (CRF-MG 24309). Atualizado em: 01 de outubro de 2025.